Причины
Среди причин развития ОРДС у взрослых выделяют легочные (прямые) и внелегочные (непрямые) факторы:
- Легочные факторы: ушибы и травмы легких, инфекционно-воспалительные заболевания, пневмоторакс, аспирация жидкости, радиационный пневмонит, легочное кровотечение, тромбоэмболия легочной артерии, отравление токсическими газами, трансплантация легкого.
- Внелегочные факторы: массивная гемотрансфузия, сепсис, ожоги, тяжелые неторакальные травмы, шок, передозировка лекарств и наркотиков, обширные операции, уремия, ДВС-синдром, онкозаболевания, панкреонекроз, системные патологии, сильное переохлаждение или перегревание, электротравма, утопление.
Основные причины развития РДС у новорожденных:
- Нарушение выработки и экскреции сурфактанта альвеолоцитами из-за незрелости тканей легких.
- Врожденный дефект структуры сурфактанта.
Предрасполагающие факторы развития РДС у ребенка:
- Дистресс плода из-за негативных внутриутробных факторов (гипоксия, гемолитическая болезнь, асфиксия в родах, преждевременная отслойка плаценты и др.);
- Пневмопатия у новорожденных (незрелость тканей легких, аспирация околоплодных вод, ателектазы, отечно-геморрагический синдром и др.);
- Преждевременные роды или кесарево сечение без родовой деятельности;
- Сахарный диабет 1-го типа у матери;
- Недоношенность;
- Асфиксия новорожденного;
- Охлаждение ребенка, гиповолемия.
История и физика
Клинический спектр COVID-19 варьируется от бессимптомных форм до состояний с дыхательной недостаточностью, требующей искусственной вентиляции легких и интенсивной терапии. В тяжелых случаях наблюдаются полиорганные проявления, такие как сепсис и синдромы полиорганной дисфункции (MODS).
В одном из первых исследований ученый Хуан отметил, что пациенты испытывали лихорадку, недомогание, сухой кашель и одышку. Компьютерная томография (КТ) грудной клетки выявила пневмонию у всех пациентов. Около трети из них (32%) нуждались в помощи в отделении интенсивной терапии, а 15% случаев завершились летальным исходом.
Исследование Ли, опубликованное в Медицинском журнале Новой Англии (NEJM) в январе 2020 года, охватило 425 первых случаев в Ухане. Средний возраст пациентов составил 59 лет (от 15 до 89 лет), при этом клинические случаи у детей младше 15 лет не были зафиксированы. Гендерные различия незначительны: 56% составили мужчины. В последующих отчетах отмечается меньшая распространенность среди женщин.
Данные Китайского центра контроля заболеваний, основанные на 72 314 историях болезни (подтвержденных, предполагаемых, диагностированных и бессимптомных случаях), были опубликованы в Журнале Американской медицинской ассоциации (JAMA). Они показали, что 62% случаев были подтверждены, включая 1% бессимптомных, но лабораторно положительных. Общая летальность составила 2,3%.
Погибали в основном пожилые пациенты, особенно в возрасте ≥ 80 лет (около 15%) и от 70 до 79 лет (8%). Примерно 49% умерших имели сопутствующие заболевания, такие как сердечно-сосудистые болезни, диабет и хронические респираторные заболевания. В группе пациентов младше 9 лет летальных случаев не было.
Авторы отчета китайского CDC классифицировали клинические проявления по степени тяжести:
- Легкое заболевание: отсутствие пневмонии и легкая пневмония – 81% случаев.
- Тяжелое заболевание: одышка, частота дыхания ≥ 30/мин, сатурация кислорода ≤ 93%, соотношение PaO2/FiO2 < 300 – 14% случаев.
- Критическое заболевание: дыхательная недостаточность, септический шок и/или полиорганная дисфункция – 5% случаев.
Согласно последующим данным, 70% пациентов имеют бессимптомное или легкое течение болезни, в то время как у 30% наблюдается респираторный синдром с высокой температурой и кашлем, что может привести к тяжелой дыхательной недостаточности.
Таким образом, клинические проявления COVID-19 можно разделить на легкие, средние и тяжелые формы. Тяжелые проявления включают пневмонию, ОРДС и системные осложнения, такие как сепсис и септический шок.
Клиническое течение болезни обычно предсказывает благоприятный исход для большинства пациентов. Однако в некоторых случаях, процент которых еще предстоит определить, через неделю может произойти резкое ухудшение состояния с дыхательной недостаточностью и MOD/MOF. Критерии степени тяжести дыхательной недостаточности и диагностические критерии сепсиса и септического шока могут служить ориентирами.
Терминальный период болезни
Четвертая стадия заболевания характеризуется прогрессирующей дыхательной недостаточностью. У пациента наблюдаются артериальная гипоксемия и гиперкапния, иногда развивается метаболический ацидоз.
Симптоматика включает:
- Профузную потливость.
- Выраженную одышку и цианоз.
- Резкое падение артериального давления, вплоть до коллапса.
- Глухость сердечных тонов, тахикардию или аритмию.
- Влажные хрипы в легких.
- Кашель с выделением пенистой мокроты розового цвета.
На ЭКГ специалист может заметить отклонение электрической оси вправо. Рентгенограмма покажет признаки повышенного давления в легочной артерии и разбухание ее корпуса.
На четвертой стадии также развивается полиорганная недостаточность. Почки функционируют с нарушениями, что может проявляться:
- Протеинурией.
- Повышенным содержанием мочевины в крови.
- Олигоанурией.
- Повышенным уровнем креатинина в крови.
- Микрогематурией.
Из-за нарушений работы печени может возникнуть легкая желтушность и повышенный уровень лактатдегидрогеназы в крови. Заболевание также негативно сказывается на работе головного мозга: пациенты отмечают заторможенность, головокружения и мигрени, возможны нарушения мозгового кровообращения.
Клиническое обследование
Для диагностики ОРДС врач будет искать ряд клинических признаков с острым началом. Он проверит вашу общую внешность, выслушает грудную клетку и измерит насыщение кислородом с помощью зонда на пальце.
Признаки ОРДС, на которые обратит внимание врач, включают:
- цианоз (синеватая окраска языка и губ);
- тахипноэ (учащенное, поверхностное дыхание);
- тахикардия (учащение пульса);
- гипоксемия (низкие уровни кислорода в крови);
- периферическая вазодилатация (расширение кровеносных сосудов на периферии);
- хрипы в груди: врач прослушает грудную клетку с помощью стетоскопа, чтобы выявить хрипящие, скрипучие или потрескивающие звуки, указывающие на нарушение работы дыхательных путей.
Как диагностируется ОРДС?
Если у вас есть подозрения на ОРДС, врач проведет ряд анализов. Необходимы общий анализ крови, тесты на функции почек и печени (печеночная проба, LFT), анализ свертываемости крови и посев крови. Эти исследования помогут выявить предрасполагающую инфекцию и оценить работу других органов.
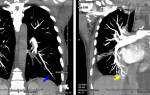
Рентгенография грудной клетки играет ключевую роль в диагностике и мониторинге заболевания. Она позволяет визуализировать накопление жидкости в легких.
Также будет регулярно измеряться уровень кислорода в крови. Могут быть проведены более специализированные исследования, например, установка катетеров для измерения артериального давления. Это поможет исключить другие причины накопления жидкости в легких, такие как застойная сердечная недостаточность.
Сепсис
Согласно международным определениям сепсиса и септического шока (Сепсис-3), сепсис — это угроза жизни, вызванная нерегулируемой реакцией организма на инфекцию, приводящая к дисфункции органов.
Клиническая картина пациентов с COVID-19 и сепсисом серьезна и включает широкий спектр признаков и симптомов, указывающих на поражение нескольких органов. К ним относятся респираторные проявления, такие как тяжелая одышка и гипоксемия, почечная недостаточность с уменьшением диуреза, тахикардия, измененное психическое состояние, а также лабораторные данные, свидетельствующие о гипербилирубинемии, ацидозе, повышенном уровне лактата, коагулопатии и тромбоцитопении.
Шкала оценки последовательной органной недостаточности (SOFA) служит эталоном для оценки полиорганного повреждения и его прогностической значимости, предсказывая смертность в ОИТ на основе лабораторных и клинических данных. Педиатрическая версия этой оценки также была проверена.
Симптомы
В клинической картине респираторного дистресс-синдрома у взрослых выделяют четыре периода.
Первый период — скрытый. Он длится сутки после контакта с этиологическим фактором. В это время происходят патофизиологические изменения, но симптомы не проявляются, и рентгенограмма остается без изменений. Однако у пациента может наблюдаться тахипноэ — более 20 дыханий в минуту.
Второй период — период начальных изменений. Он фиксируется на 1-2 сутки после воздействия фактора. Начинают проявляться симптомы: тахикардия и выраженная одышка. Аускультация выявляет жесткое везикулярное дыхание и рассеянные сухие хрипы. На рентгенограмме отмечается усиление сосудистого рисунка, особенно в периферических отделах, что указывает на начало интерстициального отека легких. Исследование газового состава крови может показать незначительное снижение РаО2.
Третий период — развернутый, или период выраженных клинических проявлений. Симптомы становятся ярко выраженными, у пациента наблюдается острая дыхательная недостаточность. В дыхании участвует вспомогательная мускулатура, заметно раздуваются крылья носа и втягиваются межреберные промежутки. Также отмечается диффузный цианоз. При аускультации сердца выявляют глухость тонов и тахикардию, артериальное давление значительно падает.
Перкуссия показывает притупленный звук, особенно в задненижних отделах, а аускультация — жесткое дыхание и иногда сухие хрипы. Появление влажных хрипов и крепитации указывает на альвеолярный отек легких, который может быть как незначительным, так и выраженным. Рентгенография демонстрирует выраженный интерстициальный отек и двусторонние инфильтративные тени неправильной формы, сливающиеся с корнями легких. РаО2 может снижаться до 50 мм рт. ст., даже при ингаляции кислорода.
Четвертый период — терминальный. В этом состоянии дыхательная недостаточность прогрессирует, развивается артериальная гипоксемия и гиперкапния, а также метаболический ацидоз. Формируется острое легочное сердце из-за нарастающей легочной гипертензии. Симптоматика включает:
- профузную потливость
- выраженную одышку и цианоз
- резкое падение артериального давления вплоть до коллапса
- глухость сердечных тонов и тахикардию, возможны аритмии
- обильные влажные хрипы и крепитацию
- кашель с пенистой мокротой розового оттенка
В этой стадии развиваются признаки легочной гипертензии и синдрома острого легочного сердца. На ЭКГ фиксируется отклонение электрической оси сердца вправо, высокие острые зубцы Р в отведениях II, III, avF, V1-2. Рентгенограмма показывает признаки повышения давления в легочной артерии.
Для четвертой стадии характерно развитие полиорганной недостаточности. Функция почек нарушается, что проявляется:
- протеинурией
- олигоанурией
- микрогематурией
- цилиндрурией
- повышением уровня мочевины и креатинина в крови
Функция печени также нарушается, что приводит к легкой желтушности и повышению уровня фруктозо-1-фосфатальдолазы, аланиновой аминотрансферазы и лактатдегидрогеназы. Нарушается работа головного мозга: пациент становится заторможенным, испытывает головокружение и головные боли, могут проявляться симптомы нарушения мозгового кровообращения. Исследование газового состава крови фиксирует гиперкапнию и глубокую артериальную гипоксемию. Анализ кислотно-щелочного равновесия выявляет метаболический ацидоз.
Лечение
Лечение направлено на борьбу с дыхательной недостаточностью и ее последствиями, ликвидацию гиалиновых мембран и поддержание гомеостаза.
Ключевое значение имеет поддержание температуры и влажности окружающей среды (кувез с температурой 32—34°). Влажность вдыхаемого воздуха обеспечивается мелкодисперсной аэрозольной взвесью, содержащей 20% раствор глицерина, лецитин для стабилизации сурфактанта и стрептазу или плазмин для растворения фибриновой матрицы гиалиновых мембран.
При апноэ (pCO2 крови более 75 мм рт. ст., pO2 крови ниже 40 мм рт. ст. с прогрессирующим снижением pH ниже 7,2) на фоне дыхания чистым кислородом эффективна искусственная вентиляция легких. Оксигенотерапия показана при всех случаях дистресс-синдрома. Процент кислорода во вдыхаемой смеси регулируется для поддержания артериального pO2 в пределах 50—70 мм рт. ст. Если этот показатель определить невозможно, содержание кислорода во вдыхаемом воздухе ежедневно уменьшается до появления цианоза, после чего концентрация кислорода увеличивается на 10%. В некоторых случаях рекомендуется оксигенобаротерапия, а при нарушении проходимости дыхательных путей — ингаляции кислородогелиевых смесей. Введение бикарбоната натрия без лабораторного контроля возможно только при стойкой брадикардии, остановке сердца или на фоне искусственной вентиляции легких (3—5 мл 5% раствора бикарбоната натрия на 1 кг веса внутривенно).
Гомеостаз поддерживается переливанием растворов солей, глюкозы и аминокислот в объемах, соответствующих суточным потребностям.
Для предотвращения внутрисосудистого свертывания и профилактики гиалиновых мембран применяется гепарин в сочетании с фибринолитическими препаратами — плазмином и стрептазой. При подозрении на внутриутробную инфекцию и для профилактики бактериальных пневмоний назначаются курсы антибиотиков.
Прогноз при современных методах лечения благоприятный.
Профилактика
Профилактика дистресс-синдрома заключается в предотвращении заболеваний и состояний, которые его вызывают. В первую очередь необходимо:
- своевременно лечить пневмонию;
- предотвращать закупорку легочной артерии эмболами, о которых говорилось в разделе, посвященном причинам болезни;
- избегать состояний, при которых в легкие попадает рвотное содержимое желудка или другие жидкости (например, вода при утоплении);
- прекратить работу на вредных производствах, связанных с вдыханием ядовитых газов и испарений;
- не заниматься альпинизмом или туризмом в высокогорных районах без физической подготовки и соответствующего снаряжения;
- качественно и быстро лечить различные виды шока (от анафилактического до септического) и нарушения метаболизма;
- проводить внутривенные вливания препаратов в соответствии с потребностями организма;
- проявлять клиническую настороженность к дистресс-синдрому при наличии аутоиммунных заболеваний, когда организм атакует собственные клетки легочной ткани;
- бросить курить, так как никотин способствует развитию дистресс-синдрома, изменяя легочную ткань, и усугубляет уже существующее состояние.
Патогенез
В основе патогенеза лежит системная воспалительная реакция в легочной ткани. На начальной стадии воспаления активно выделяются эндотоксины, интерлейкин-1, фактор некроза опухоли и другие провоспалительные цитокины. Затем в процесс вовлекаются лейкоциты и тромбоциты, активированные цитокинами, которые локализуются в интерстиции, капиллярах и альвеолах, начиная выделять медиаторы воспаления (протеазы, кинины, свободные радикалы, активирующие комплемент, нейропептиды). Эти медиаторы увеличивают проницаемость капилляров легких для белка, что приводит к снижению онкотического давления между интерстициальной тканью и плазмой и выходу жидкости из сосудов, вызывая отек альвеол и интерстициальной ткани. Эндотоксины играют ключевую роль, нанося прямое повреждение клеткам эндотелия легочных капилляров и увеличивая активность медиаторных систем организма.
Повышенная проницаемость капилляров легких, даже при незначительном увеличении гидростатического давления, усиливает альвеолярный и интерстициальный отек, особенно в нижних отделах легких. Это нарушает газообмен, что усугубляется ателектазом из-за снижения активности сурфактанта. Резкое снижение вентиляции при сохраненной перфузии и шунтировании крови приводит к гипоксемии и гипоксии. Шунтирование происходит из-за попадания венозной крови, не обогащенной кислородом, в артериальное русло через ателектазированные участки легких и альвеолы, заполненные жидкостью.
Увеличение мертвого пространства из-за окклюзии легочных капилляров также нарушает газообмен. Снижение эластичности легких требует увеличения усилий дыхательных мышц, что приводит к их утомлению и дополнительной дыхательной недостаточности.
Повреждения легких в течение 2-3 суток переходят во вторую морфологическую фазу, характеризующуюся бронхоальвеолярным и интерстициальным воспалением, а также пролиферацией интерстициальных и эпителиальных клеток. Третья фаза характеризуется быстрым развитием коллагена, что в течение 15-20 суток приводит к тяжелому пневмофиброзу с формированием мелких воздушных кист в паренхиме легких.
Таким образом, для патологического процесса при ОРДС характерна стадийность, выделяющая несколько патоморфологических фаз:
- Острая фаза (2-4 суток) – поражение эпителия альвеол и капилляров, альвеолярный и интерстициальный отек, развитие микроателектазов. При благоприятном течении явления постепенно стихают, транссудат рассасывается; при неблагоприятном – происходит переход в подострую или хроническую фазу.
- Подострая фаза – развитие интерстициального и бронхоальвеолярного воспаления.
- Хроническая фаза – развитие выраженного фиброзирующего альвеолита, характеризующегося уплощением и утолщением капиллярно-альвеолярных мембран, разрастанием соединительной ткани, формированием микротромбозов и запустеванием сосудистого русла.
Этиология
ОРДС возникает из-за прямого или непрямого повреждения лёгких. Непрямое повреждение связано с системной воспалительной реакцией при внелёгочных заболеваниях. Наиболее частыми причинами являются сепсис, пневмония (включая аспирационную) и тяжёлые травмы. Другие причины представлены в таблице.
| Прямое повреждение лёгких | Непрямое повреждение лёгких |
|---|---|
| Аспирация | Сепсис |
| Пневмония | Тяжёлая травма |
| Диффузное альвеолярное кровотечение | Пересадка костного мозга |
| Жировая эмболия | Ожоги |
| Пересадка лёгких | Кардиопульмональный шунт |
| Утопление | Передозировка лекарств (аспирин, кокаин, опиоиды, фенотиазины, трициклические антидепрессанты) |
| Ушиб лёгкого | Массивное переливание крови |
| Вдыхание токсичных газов и аэрозолей | Панкреатит |
| Вдыхание радиоактивных газов и аэрозолей (например, аэрозолей с полонием-210). В случае выживания выздоровление может занять много лет из-за медленного распада полония-210. | Рентгеноконтрастные препараты (редко) |
Признаки РДСВ
Клиническая картина токсического отека легких развивается в течение 12-48 часов после повреждения организма.
Симптомы нарастают быстро. Первым признаком обычно является одышка с частым поверхностным дыханием. Кожные покровы становятся сначала бледными, затем цианотичными.
Объективные данные на этом этапе скудны:
- В легких не всегда выявляются патологические симптомы.
- У некоторых больных может отмечаться ослабленное дыхание с единичными сухими или влажными хрипами.
- Рентгенография показывает диффузное усиление легочного рисунка, а лабораторные исследования — снижение парциального давления кислорода в крови.
Эти признаки должны насторожить врача, особенно при отсутствии заболеваний легких в анамнезе.
С прогрессированием болезни состояние больных ухудшается:
- В легких нарушается синтез сурфактанта, альвеолы спадаются, что приводит к тяжелой дыхательной недостаточности.
- Над легкими появляются рассеянные влажные хрипы, дыхание становится клокочущим.
- На рентгенограмме определяется снижение пневматизации легочной ткани по типу «снежной бури».
На этом этапе к РДСВ может присоединиться бактериальная инфекция, что усугубляет течение болезни.
Характерной чертой токсического отека легких является несоответствие между рентгенологической картиной и функциональными нарушениями. Артериальная гипоксемия может быть непропорционально тяжелой по сравнению с видимым отеком легких.
РДСВ имеет свои особенности при различных состояниях и заболеваниях:
- При вдыхании токсических аэрозолей или дыма возникает приступообразный кашель и чувство саднения в горле. Затем наступает период мнимого благополучия, который может длиться несколько часов или дней. В дальнейшем состояние резко ухудшается: усиливается кашель, нарастает одышка и проявляется отек легких.
- При сепсисе и других инфекционных заболеваниях РДСВ развивается на фоне инфекционно-токсического шока, что усугубляет состояние пациентов.
- При тяжелых аллергических реакциях дыхательная недостаточность сопровождается кожными проявлениями, гипотензией и гипертермией. В этом случае причиной является отек легких, а не бронхоспазм.
Эндотрахеальная интубация и инвазивная ИВЛ
Интубация трахеи и инвазивная искусственная вентиляция легких при ОРДС показаны в следующих случаях:
- Апноэ
- Остановка кровообращения
- Нарушение сознания (возбуждение, делирий, оглушение, сопор, кома)
- Нарушение глоточных рефлексов
- Нарушение кашлевого рефлекса
- Парез голосовых складок
Эндотрахеальную интубацию следует проводить при полном отсутствии дыхания (апноэ, остановка кровообращения). Она также показана при высоком риске аспирации (делирий, нарушение сознания) и нарушении функции голосовых складок. Рандомизированные контролируемые исследования по оценке абсолютных показаний для искусственной вентиляции легких не проводились по этическим соображениям.
В большинстве случаев абсолютные показания к интубации (нарушение глоточных рефлексов, нарушение сознания, парез голосовых складок) связаны с другими состояниями, такими как травма, шок, сепсис, полинейропатия критических состояний и полиорганная недостаточность.
Многие пациенты с ОРДС нуждаются в эндотрахеальной интубации и инвазивной искусственной вентиляции как по абсолютным, так и по относительным показаниям, поскольку эти меры могут улучшить исход.
Исследования по относительным и абсолютным показаниям к респираторной поддержке не проводились по этическим причинам. Представленные показания основаны на экспертном консенсусе, опубликованном в 1993 году:
- Участие вспомогательной мускулатуры в дыхании
- Частота дыхания > 35 (у взрослых)
- Гипоксемия (SpO2 < 90% или PaO2 < 60 мм рт. ст. несмотря на ингаляцию кислорода) и/или гиперкапния
- Нарушения гемодинамики
В крупном мультицентровом исследовании 85% пациентов с ОРДС были интубированы и подключены к ИВЛ, большинство из них в первые 24 часа после появления первых признаков заболевания. Перед интубацией средний показатель PaO2/FiO2 у этих пациентов составлял 146±84 мм рт. ст., при этом у 74% наблюдался шок или необходимость в катехоламиновой поддержке.
В другом исследовании 70% пациентов с ОРДС были интубированы изначально. У 30% применялась неинвазивная искусственная вентиляция легких, но в 46% случаев она оказалась неэффективной. В итоге частота проведения инвазивной ИВЛ составила 84%.
Заключение
Лечение токсического отека легких представляет собой сложную задачу для врачей. Это обусловлено разнообразием патогенетических механизмов, поздней диагностикой и отсутствием эффективных терапевтических методов. Прогноз остается неблагоприятным, и летальность достигает 40-60%, несмотря на проводимую терапию. В настоящее время продолжается разработка новых методов лечения и технологий респираторной поддержки.
При быстром эффекте от лечения остаточные нарушения легочной функции и трудоспособности обычно выражены слабо или отсутствуют. У большинства выживших функциональные признаки фиброза исчезают в течение нескольких месяцев.
Наглядно о РДСВ: