Прогнозировование и факторы риска при миеломе
«Международная система прогнозирования» (ISS, 2005) была разработана на основе данных о естественном течении заболевания у значительной группы пациентов и исследования бета-2-микроглобулина в динамике. У 75% больных миеломной болезнью уровень бета-2-микроглобулина повышен.
Выделяются три уровня этого онкомаркера, которые связаны с выживаемостью пациентов и позволяют определить стадии заболевания:
- Бета-2-микроглобулин менее 3,5 мг/л и альбумин более 35 г/л — средняя выживаемость 62 месяца.
- Промежуточный уровень между 1 и 3 стадиями — средняя выживаемость 44 месяца.
- Бета-2-микроглобулин более 5,5 мг/л — средняя выживаемость 29 месяцев.
Тем не менее, новые препараты значительно изменили прогноз заболевания. Международная система была протестирована для новейшей терапии и подтвердила свою надежность. 5-летняя выживаемость больных на стадиях I, II и III составила 66%, 45% и 18% соответственно.
В Международной системе не учтены важные прогностические показатели, такие как число тромбоцитов, уровень лактатдегидрогеназы и свободных легких цепей в крови. Число тромбоцитов коррелирует с вытеснением костного мозга и имеет предсказательное значение выше, чем альбумин. Уровень лактатдегидрогеназы (ЛДГ) связан с общей массой миеломных клеток, недостаточным ответом на терапию и укорочением выживаемости. У больных с уровнем свободных легких цепей выше 4,75 г/л чаще наблюдается почечная недостаточность, высокий процент миеломных клеток в пунктате костного мозга, а также высокие значения бета-2-микроглобулина и ЛДГ. Эти показатели также связаны с болезнью отложения легких цепей и III стадией по Международной системе. Однако представленных доказательств оказалось недостаточно для их включения в систему. Тем не менее, они были учтены в системе Дьюри-Саймона (1975), значение которой остается актуальным.
Повышенный уровень сывороточного бета-2-микроглобулина, лактатдегидрогеназы и низкий уровень альбумина считаются неблагоприятными прогностическими признаками при миеломной болезни. Хотя уровень бета-2-микроглобулина увеличивается при почечной недостаточности, существует значительная корреляция между объемом опухолевой ткани и концентрацией этого биомаркера в крови, за исключением случаев, когда миеломная болезнь развивается на фоне уже имеющейся почечной недостаточности.
Перспективным методом оценки прогноза заболевания является генетическое исследование опухоль-ассоциированных генов. Цитогенетическое выявление транслокаций, в отличие от трисомии, относится к неблагоприятным прогностическим признакам. Метод флюоресцентной гибридизации in situ (FISH) упростил выявление хромосомных аберраций в миеломных клетках. Исследователи клиники Мэйо (США) предлагают использовать этот метод для выбора индивидуальной лечебной тактики на основе выявленных аберраций. Генетические исследования хромосомных аномалий и мутаций при миеломе являются перспективными для лабораторной оценки прогноза и устойчивости к терапии. Однако для их оценки требуется больше времени и данных о большем числе пролеченных больных, чтобы определить, способны ли новые терапевтические средства преодолеть цитогенетические показатели высокого риска при миеломной болезни.
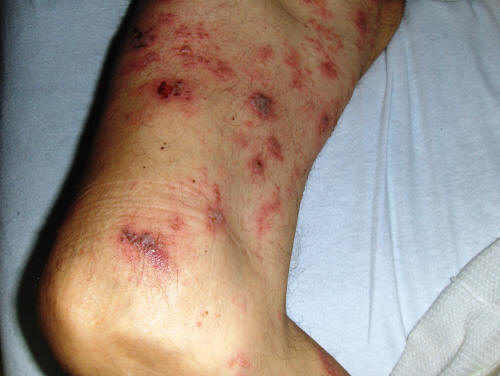
Миеломная болезнь – симптомы
Миеломная болезнь чаще всего развивается у пожилых людей, затрагивая как женщин, так и мужчин. Болезнь Рустицкого-Калера проявляется следующими симптомами и клиническими признаками:
- поражение кроветворной и костной систем;
- нарушение обменных процессов;
- изменения в мочевыделительной системе.
Симптомы множественной миеломы:
- первые признаки — боль в костях (в позвоночнике, грудной клетке, черепе), спонтанные переломы, деформация костей и опухолевые образования;
- частые пневмонии и другие заболевания из-за снижения иммунитета и ограниченных дыхательных движений, вызванных изменениями в костях грудной клетки;
- дистрофические изменения в сердечной мышце, сердечная недостаточность;
- увеличение селезенки и печени;
- миеломная нефропатия — нарушение функции почек с повышением белка в моче, что может привести к почечной недостаточности;
- нормохромная анемия — снижение количества эритроцитов и уровня гемоглобина;
- гиперкальциемия — повышенное содержание кальция в плазме и моче, что опасно и проявляется рвотой, тошнотой, сонливостью, нарушениями вестибулярного аппарата и психическими расстройствами;
- снижение уровня нормального иммуноглобулина;
- нарушения кроветворения — кровоточивость слизистых, появление синяков, спазмы артерий фаланг, геморрагический диатез;
- парестезии («мурашки»), головные боли, сонливость, переходящая в ступор, судороги, головокружение, глухота, одышка;
- на последних стадиях — снижение веса, повышение температуры тела, тяжелая анемия.
Формы миеломной болезни
По клинико-анатомической классификации миеломная болезнь делится на следующие формы:
- солитарная миелома – один опухолевый очаг в кости или лимфоузле;
- множественная (генерализованная) миелома – несколько опухолевых очагов.
Множественная миелома может быть:
- диффузной – патологические образования пронизывают всю структуру костного мозга без четких границ;
- множественно-очаговой – плазмоцитома развивается на ограниченных участках, также опухоли могут возникать в лимфатических узлах и селезенке;
- диффузно-очаговой – сочетает признаки диффузной и множественной миеломы.
Миеломная болезнь – стадии
Врачи выделяют три стадии множественной миеломы. Вторая стадия является переходной, с показателями выше первой, но ниже третьей (самой тяжелой):
- Первая стадия: гемоглобин понижен до 100 г/л, уровень кальция нормальный, низкая концентрация парапротеинов и белка Бенс-Джонса, один опухолевый очаг размером 0,6 кг/м², отсутствие остеопороза и деформации костей.
- Третья стадия: гемоглобин понижен до 85 г/л и ниже, уровень кальция в крови выше 12 мг на 100 мл, множественные опухоли, высокая концентрация парапротеинов и белка Бенс-Джонса, общий размер опухоли 1,2 кг/м² и более, явные признаки остеопороза.
Осложнения миеломной болезни
Для множественной миеломы характерны осложнения, вызванные разрушительной деятельностью опухоли:
- сильные боли и переломы костей;
- почечная недостаточность, требующая гемодиализа;
- частые инфекционные заболевания;
- тяжелая анемия, требующая переливаний.
Симптомы множественной миеломы
Миеломная болезнь имеет длительное течение. От первых симптомов до ярких клинических проявлений проходит 10-20 лет.
- Костно-мозговой синдром проявляется лизисом костей, преимущественно позвоночника, плоских и проксимальных отделов трубчатых костей. Дистальные отделы поражаются редко. Больные жалуются на боли в костях и частые переломы. При перкуссии отмечается боль в конечностях.
- Триада Калера (остеопороз со спонтанными переломами, болью и опухолями) характерна для этих пациентов.
- Нарушения в работе центральной нервной системы могут привести к параплегии, слабости и утомляемости. Из-за отложения амилоида в костях черепа возможны нарушения работы черепных нервов. Характерно поражение периферических нервов конечностей и снижение чувствительности по типу «перчаток и носок», а также отсутствие чувствительности в дистальных отделах конечностей.
- Почечная недостаточность может быть вызвана высоким уровнем белка M в организме.
- Синдром иммуноглобулинопатии. Начинает синтезироваться амилоидный белок, который активно реабсорбируется почками, повреждая их. В моче нарастает протеинурия (белок Бенс-Джонса). Постепенно снижается концентрационная и фильтрационная функция почек, появляются отеки и положительный симптом поколачивания (боли в пояснице при поколачивании кулаком).
- Синдром иммунодефицита. Нормальный белок заменяется патологическим, что нарушает синтез антител и компонентов иммунной системы. В результате нарастает дефект гуморального иммунитета, и пациенты становятся уязвимыми к бактериальным и вирусным инфекциям. Часто возникают оппортунистические инфекции.
- Синдром повышенной вязкости: повышенная кровоточивость, синдром Рейно (нарушение микроциркуляции в дистальных сегментах конечностей), кровоизлияния в сетчатку, снижение кровоснабжения головного мозга, возможное развитие ДВС-синдрома.
- Гиперкальциемия. Повышенная активность остеокластов приводит к выделению большого количества кальция в кровь. Симптомы гиперкальциемии: тошнота, рвота, судороги. Характерны нарушения сердечной проводимости: увеличение интервала QRS и Т, снижение АВ-проводимости, вплоть до АВ-блокады. Образование камней в почках связано с отложением кальция, что снижает фильтрацию и реабсорбцию, в результате почка сморщивается.
- Поражение внутренних органов: спленомегалия, гепатомегалия, язвенное поражение желудка. В различных органах и тканях откладывается амилоид, что нарушает их работу. Боли в сердце, расширение границ сердечной тупости и глухость тонов также характерны. Боли в мышцах могут быть постоянными.
- Анемический синдром. Опухолевые клетки вытесняют нормальный росток кроветворения, что приводит к снижению уровня гемоглобина и эритроцитов. Кожные покровы становятся бледными и покрываются кровянистыми пятнами, возникает постоянное чувство слабости. Волосы и ногти становятся ломкими.
Какие тесты используются специалистами здравоохранения для диагностики множественной миеломы?
У многих пациентов множественная миелома впервые подозревается при обычном анализе крови, который показывает аномальное количество белка или повышенную липкость красных кровяных клеток. Это приводит к образованию структур, напоминающих монеты, называемых rouleaux. Медицинский работник проводит сбор анамнеза и физикальное обследование, ища признаки и симптомы множественной миеломы.
Если диагноз вызывает подозрение, для его подтверждения выполняются несколько исследований. К ним относятся аспирация костного мозга и биопсия, чаще всего из крупных костей таза. Полученные клетки анализируются патологом на наличие аномальных типов или количества клеток (плазмацитома или множественная миелома). Также изучается образец костного мозга на наличие аномальных хромосом (цитогенетическое тестирование). Дополнительные молекулярные тесты могут быть проведены на образце костного мозга. Биопсия позволяет оценить концентрацию клеток и наличие аномального роста.
Анализы крови и мочи, включая уровень креатинина в сыворотке, помогают определить уровни и типы моноклонального белка и оценить повреждение почек. М-белок может быть полной формой антитела (иммуноглобулин, например, IgG или IgA) или его частью (легкая цепь лямбда или каппа). Нормальные антитела состоят из тяжелой и легкой цепей. В 2011 году Национальная комплексная онкологическая сеть (NCCN) рекомендовала использовать бесклеточный анализ легкой цепи и флуоресцентную гибридизацию in situ (FISH) для выявления множественной миеломы.
Большинство клиницистов используют рентгенологические исследования для выявления повреждений скелета и МРТ для оценки поражений спинного и параспинального мозга. Также проводятся стандартные тесты, такие как общий анализ крови (CBC), скорость оседания, уровень азота мочевины в крови (BUN), C-реактивный белок и другие. Белки Бенса-Джонса, моноклональные полипептиды легких цепей антител, могут быть обнаружены в моче с помощью иммунофиксации на электрофоретическом геле.
Причины и патогенез миеломной болезни
Причины миеломы неизвестны, но есть факторы, повышающие риск заболевания:
- Возраст. До 40 лет миелома встречается редко, после 70 лет риск значительно возрастает.
- Пол. Мужчины болеют чаще женщин.
- Раса. У людей с черным цветом кожи риск миеломы в два раза выше, чем у европейцев или азиатов.
- Моноклональная гаммапатия. У 1 из 100 человек она может трансформироваться в множественную миелому.
- Семейная история. Наличие случаев миеломы или гаммапатии в семье увеличивает риск.
- Иммунные патологии. ВИЧ или применение иммунодепрессантов повышают вероятность заболевания.
- Воздействие токсинов. Радиоактивное излучение, пестициды и удобрения могут способствовать развитию миеломы.
В норме костный мозг вырабатывает определенное количество В-лимфоцитов и плазматических клеток. При миеломе этот процесс выходит из-под контроля: костный мозг заполняется аномальными плазматическими клетками, что снижает образование нормальных лейкоцитов и эритроцитов. Вместо антител, необходимых для борьбы с инфекциями, такие клетки производят белки, способные повреждать почки.
СМОТРЕТЬ ДРУГИЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
(Сокращённый вариант) Год утверждения: 2020
Профессиональные ассоциации:
- Общероссийский национальный союз «Ассоциация онкологов России»
- Некоммерческое партнерство «Национальное гематологическое общество»
- Региональная общественная организация «Общество онкогематологов»
Одобрено Научно-практическим Советом Минздрава РФ
Оглавление:
- Краткая информация
- Диагностика
- Лечение
- Реабилитация
- Профилактика
- Организация оказания медицинской помощи
- Дополнительная информация
Классификация форм плазмоцитомы
Классификация миеломы основывается на локализации новообразования и клеточном составе опухоли.
Существует два основных типа миеломы:
- Множественная миелома. Злокачественные новообразования формируются в нескольких участках костей и поражают костный мозг. Это приводит к вовлечению лимфатических узлов и селезенки. Плазмоцитомы чаще всего локализуются в позвоночнике, черепе, лопатках, ребрах, длинных костях конечностей и подвздошных крыльях.
- Солитарная (единичная) плазмоцитома. Обнаруживается в одном месте — в костях или лимфоузле.
Наиболее распространенной является множественная миелома. Симптомы и методы лечения схожи для обоих типов, но определение формы важно для точного диагноза и прогнозирования течения заболевания.
По месторасположению очагов выделяют:
- Диффузная миелома. Атипичные клетки распределены по всему костному мозгу.
- Множественно очаговая миелома. Злокачественные очаги увеличивают объем костного мозга.
- Диффузно-множественная миелома. Объединяет симптомы диффузной и множественной плазмоцитомы.
Диффузно-множественная миелома подразделяется на три типа в зависимости от клеточного состава:
- Плазмоклеточная миелома. Преобладают зрелые плазмоциты, активно синтезирующие парапротеины, что приводит к затяжному и трудно поддающемуся лечению заболеванию.
- Плазмобластная миелома. Преобладают плазмобласты, синтезирующие небольшое количество парапротеинов. Заболевание быстро прогрессирует, но лучше поддается лечению.
- Мелкоклеточная и полиморфная миеломы. Пораженные плазмоциты выявляются на ранних стадиях, что указывает на тяжелую патологию и сложность лечения.
Также различают острую и хроническую формы заболевания. Острая форма характеризуется быстрым развитием и ускоренным ростом атипичных клеток, что приводит к распространению плазмоцитов в другие органы и ткани. Хроническая форма, наоборот, развивается медленно и поражает только костные ткани.
Суть заболевания
Плазматические клетки — это лейкоциты, образующиеся из В-лимфоцитов, которые вырабатывают иммунные антитела. Они находятся в костном мозге, лимфоузлах, кишечнике и миндалинах. В норме плазмоциты составляют не более 5% от общего числа клеток костного мозга. Если их количество превышает 10%, это может указывать на патологию.
Основная функция плазматических клеток — синтез иммуноглобулинов для защиты организма в биологических жидкостях: крови, лимфе и слюне. За одну секунду они производят несколько сотен антител.
При сбое на этапе созревания В-лимфоцитов вместо плазматической клетки образуется миеломная клетка с злокачественными свойствами. Название связано с тем, что патологический процесс чаще всего развивается в костном мозге.
Все миеломные клетки происходят из одной мутировавшей клетки, которая активно размножается. Их скопление называется плазмоцитомой и может обнаруживаться в костях и мышцах.
Опухолевая клетка формируется в костном мозге и прорастает в кость, где начинает клонироваться. Их количество быстро растет, и в кровь проникают патологические иммуноглобулины — парапротеины. Эти молекулы не участвуют в иммунной реакции и откладываются в тканях, что можно увидеть в анализах крови.
При миеломе в костях и позвонках образуются пустоты различной величины и локализации. Злокачественные клетки внутри костной ткани стимулируют остеокласты, которые разрушают хрящи и кости, оставляя пустоты. Они также выделяют цитокины, которые негативно влияют на здоровье, так как:
- способствуют размножению миеломных клеток, что приводит к образованию новых патологических очагов;
- подавляют иммунную систему, делая её уязвимой для бактериальных инфекций;
- активизируют остеокласты, что ослабляет кости и увеличивает риск переломов;
- стимулируют образование фибробластов, что приводит к сгущению крови и появлению синяков;
- вызывают рост гепатоцитов, что нарушает выработку протромбина и фибриногена, ухудшая свёртываемость крови;
- изменяют белковый обмен, что может повредить почки, особенно при миеломе Бенса-Джонса.
Отек костного мозга позвоночника.
Классификация миеломных заболеваний
Солитарная миелома. Этот вид заболевания характеризуется опухолевым очагом, локализующимся на одной из костей, заполненных костным мозгом, или в узле лимфатической системы. Это отличает солитарную миелому от других форм, где опухолевые очаги располагаются в двух или трех костях.
Множественная миелома. В этом случае опухолевые очаги формируются одновременно в двух или трех костях с костным мозгом. Чаще всего поражаются позвонки, ребра, лопатки, череп, крылья подвздошной кости и кости конечностей. Также затрагиваются лимфатические узлы и селезенка. Множественная миелома встречается чаще, чем солитарная.
Специалисты различают эти формы для точной диагностики и прогноза лечения. В зависимости от локализации миелома делится на диффузно-очаговую и множественно-очаговую.
Диффузная миелома. В этом случае плазматические клетки прогрессивно увеличиваются в количестве. Ограниченных очагов нет, и плазмоциты проникают в структуры костного мозга, распределяясь по всей его поверхности.
Множественно-очаговая миелома. Здесь наблюдается активный очаг развития клеток, продуцирующих антитела, что приводит к изменению структуры костных соединений. Эти клетки локализуются на определенном участке, формируя очаг новообразования, в то время как другие участки деформируются.
Диффузно-очаговая миелома. Сочетает свойства диффузной и множественной форм. По клеточному составу миелома делится на плазмоцитарную, плазмобластную, полиморфноклеточную и мелкоклеточную.
Плазмоклеточная миелома. В этом варианте преобладают зрелые клетки, активно вырабатывающие антитела и парапротеины. Заболевание развивается медленно, но из-за высокой продукции парапротеинов миелома может поражать другие органы и системы, что затрудняет лечение.
Плазмобластная миелома. Здесь преобладают плазмобласты — активно размножающиеся клетки, секретирующие парапротеины. Эта форма миеломы быстро растет и прогрессирует, но легче поддается лечению.
Полиморфноклеточная и мелкоклеточная миелома. Эти формы характеризуются наличием плазмоцитов, находящихся на начальной стадии развития. Они считаются наиболее злокачественными и развиваются стремительно.
Что такое лечение множественной миеломы?
Существует неизвестное лечение, которое полностью излечивает множественную миелому. Однако существуют методы, позволяющие уменьшить симптомы и продлить жизнь. Терапия определяется в зависимости от состояния пациента и группы, занимающейся лечением рака. Команда, вероятно, будет включать специалистов по миеломе, онкологов, лучевых онкологов и других консультантов. Онкологические медсестры и другие сотрудники также играют важную роль в лечении.
Варианты лечения часто включают комбинации препаратов, которые могут назначаться в виде таблеток или вводиться внутривенно. К ним относятся лекарства, влияющие на иммунную систему, стероиды и химиотерапевтические препараты. Обычно используются комбинации этих средств. В некоторых случаях может быть рекомендована высокодозная химиотерапия с последующей трансплантацией стволовых клеток. При принятии решения о трансплантации учитываются различные факторы. Дополнительную информацию можно найти в Руководстве по национальной комплексной онкологической сети (NCCN.org), которое обновляется не реже одного раза в год. Другие медицинские процедуры могут включать стероиды, бисфосфонатную терапию, переливание крови или тромбоцитов, аутотрансплантацию и плазмаферез, в зависимости от стадии заболевания. Исследователи также используют метаанализы для определения лучших протоколов лечения.
Болезненные участки повреждения костей можно лечить лучевой терапией, а сломанные кости иногда восстанавливаются хирургически.
Существует множество препаратов для лечения множественной миеломы. Часто используются следующие лекарства в комбинации с дексаметазоном, который может назначаться перорально или внутривенно:
- Дексаметазон (Декадрон) — модуляция иммунных клеток
- Бортезомиб (Velcade) — ингибитор протеазы
- Леналидомид (Revlimid) — модуляция иммунных клеток
- Памидроновая кислота (Aredia) — ингибирует резорбцию кости
- Золедроновая кислота (Zometa) — ингибирует резорбцию кости
- Мелфалан (Alkeran) — алкилирующий агент, токсичный для клеток миеломы
- Карфилзомиб (Kyprolis) — ингибитор протеазы, одобренный FDA для пациентов без предыдущего лечения
- Дартумаб (Darzalex) — моноклональное антитело, повреждающее или убивающее клетки миеломы с белком CD38 на поверхности
- Элотузумаб (Empliciti) — активирует естественные клетки-убийцы для уничтожения клеток миеломы, обычно в сочетании с Revlimid и Дексаметазоном
Существует также семь или восемь других препаратов, которые могут использоваться отдельно или в комбинации с переливанием, хотя эффекты переливания временные. Исследования продолжаются, и новые препараты и комбинации активно изучаются. Большинство специалистов, занимающихся лечением рака, осведомлены о новейших методах лечения множественной миеломы (например, Procrit, Revlimid, Kyprolis). Кроме того, ваш врач может помочь справиться с побочными эффектами (например, тошнотой и рвотой) от химиотерапии. Одной из целей лечения является выживаемость без прогрессирования, то есть продолжительность жизни пациента без ухудшения симптомов после лечения. Также изучается низкодозовая терапия для пожилых пациентов с множественной миеломой.
Симптомы миеломной болезни
Симптомы:
- Боли в костях. Миеломные клетки образуют полости в костной ткани, богатой болевыми рецепторами. Это вызывает ноющую боль, которая усиливается при повреждении надкостницы.
- Боли в сердце, суставах и мышечных сухожилиях. Они связаны с отложением патологических белков, которые нарушают функционирование органов и раздражают чувствительные рецепторы.
- Патологические переломы. Злокачественные клетки создают пустоты в костях, что приводит к остеопорозу. Кости становятся хрупкими и ломаются даже при незначительной нагрузке. Чаще всего происходят переломы бедренных костей, ребер и позвонков.
- Снижение иммунитета. Функция костного мозга нарушается, и он вырабатывает недостаточно лейкоцитов, что угнетает защитные силы организма. Уменьшается количество нормальных иммуноглобулинов в крови, что приводит к частым бактериальным инфекциям, таким как отит, ангина и бронхит. Эти болезни затяжные и плохо поддаются лечению.
- Гиперкальциемия. Из разрушенной костной ткани в кровь попадает большое количество кальция. Это вызывает запоры, боль в животе, тошноту, частое мочеиспускание, эмоциональные расстройства, слабость и заторможенность.
- Нарушение функции почек. Миеломная нефропатия возникает из-за отложения кальция в почечных протоках в виде камней и нарушения белкового обмена. Парапротеины, вырабатываемые раковыми клетками, откладываются в канальцах нефронов, что приводит к нефросклерозу. Также нарушается отток мочи, что вызывает застой жидкости в почечных чашечках и лоханках, атрофируя паренхиму органа. При этом отеки отсутствуют, артериальное давление не повышено.
- Анемия, преимущественно нормохромная. Цветовой показатель (соотношение гемоглобина к количеству эритроцитов) остается в норме (0,8 — 1,05). Повреждение костного мозга снижает выработку эритроцитов и, соответственно, концентрацию гемоглобина. Это приводит к кислородному голоданию клеток, что проявляется быстрой утомляемостью, снижением концентрации внимания, одышкой, сердцебиением, головной болью и бледностью кожи при нагрузке.
- Нарушения свертываемости крови. Повышение вязкости плазмы приводит к спонтанному склеиванию эритроцитов, что может вызвать образование тромбов. Снижение уровня тромбоцитов (тромбоцитопения) приводит к спонтанным кровотечениям, таким как носовые и десенные. Повреждение мелких капилляров вызывает появление синяков и кровоподтеков.
Причины миеломной болезни
Болезнь Рустицкого-Калера изучена, но причины ее возникновения остаются спорными. У больных часто обнаруживаются лимфатические вирусы Т или В типа. Поскольку В-лимфоциты превращаются в плазмоциты, любое нарушение этого процесса может привести к образованию патоплазмацитов.
Кроме вирусной теории, есть данные о том, что миеломная болезнь может быть вызвана радиоактивным облучением. Исследования людей, пострадавших в Хиросиме и Нагасаки, а также в зоне Чернобыльской АЭС, показали, что среди тех, кто получил высокие дозы облучения, наблюдается повышенный процент заболевших миеломой и другими болезнями кровеносной и лимфатической систем.
К негативным факторам, увеличивающим риск миеломной болезни, относятся:
- курение — чем дольше стаж и больше количество выкуриваемых сигарет, тем выше риск;
- иммунодефицит;
- воздействие токсичных веществ;
- генетическая предрасположенность.
Современная терапия миеломы
Терапия миеломной болезни включает следующие мероприятия:
- Лучевая и химиотерапия с использованием цитостатиков.
- Лечение анаболическими стероидами и глюкокортикостероидами.
- Хирургическое и ортопедическое вмешательство.
- Лечебная физкультура (ЛФК).
- Профилактика метаболических нарушений.
Химиотерапия
Показаниями для цитостатического лечения являются выраженные симптомы заболеваний: патологические переломы, боли, анемия, гиперкальциемия и синдром повышенной вязкости. При увеличении опухолевой массы, обострении болей и росте количества патологических плазмоцитов необходимо немедленно начинать терапию.
В день лечения потребуется пройти полное обследование, чтобы врач мог оценить стадию и форму опухолевого процесса. Для некоторых химиопрепаратов важно исключить противопоказания. Результаты исследований помогут врачу определить эффективность лечения.
Первый этап химиотерапии включает препараты циклофосфата, сарколизина и производные нитрозомочевины. Они эффективны при наличии очагов опухолевого роста плазмоцитов в количестве 2-10%.
Схемы приема и препараты подбираются индивидуально, так как невозможно предсказать реакцию опухоли на конкретное средство.
Некоторые препараты имеют серьезные противопоказания и требуют осторожности при применении.
Цитостатическая химиотерапия основывается на следующих принципах:
- Подбор комплекса препаратов.
- Использование оптимальной схемы с соблюдением сроков и дозировок.
- При прогрессировании заболевания — адекватный переход на другой препарат.
Лучевое облучение
При органических опухолях костей, миеломе и узлах в мягких тканях костного мозга и позвоночнике, а также при угрозе патологических переломов назначается лучевая терапия. На терминальной стадии, когда организм не реагирует на химиотерапию, облучение становится единственным средством помощи.
При инфекционных осложнениях антибиотикотерапия проводится по стандартным протоколам: выбираются антибиотики и выполняется посев биологических образцов. Важно помнить, что на фоне инфекции у пациентов с миеломой может развиться острая почечная недостаточность. Поэтому к антибиотикам добавляют кровезаменители, рекомендуют обильное потребление жидкости и контролируют суточный диурез и артериальное давление.
Соблюдение диеты
Специальной диеты для миеломной болезни не существует. Врачи индивидуально составляют рацион, учитывая степень заболевания и результаты обследования.
Разрушение костей и остеопороз требуют поступления кальция, поэтому рекомендуются молочные продукты. При анемии рацион должен включать железо и белок, поэтому полезно добавить печень и мясо. Почечная недостаточность часто сопутствует этому заболеванию. Для больных миеломой наиболее подходящей является бессолевая диета (стол №7).
Народные средства
При миеломной болезни народные средства могут использоваться только как дополнение к основному лечению. Это серьезное заболевание, и полагаться исключительно на рецепты народной медицины нецелесообразно. Самолечение может привести к негативным последствиям. Все приемы трав и настоев должны быть согласованы с лечащим врачом-онкологом.
Вот несколько рецептов:
-
В стакане кипятка заварите 1 ч. ложку вероники лекарственной. Настой должен настояться пару часов. Принимайте по 100 мл за час до еды и через час после нее.
-
Заварите 1 ч. ложку сухого донника лекарственного в стакане кипятка. Полученный настой принимайте перед едой по 50 мл.
Фитотерапевты отмечают, что миелома не переносит чернокорня лекарственного, лабазника вязолистного и окопника обыкновенного. Эти растения могут продлить жизнь и улучшить общее состояние, особенно при вялотекущей форме болезни, когда опухоль находится в костном мозге и не распространилась за его пределы.