Расшифровка иммунограммы у детей
Анализ крови на иммунитет у ребенка включает множество показателей. Их значения представлены в таблице:
| Показатель | Норма (X*10^9 шт. на литр) |
|---|---|
| Клеточное звено иммунитета | |
| Цитотоксические Т-клетки | 0,3-0,9 |
| Т-хелперы | 0,45-0,86 |
| Т-супрессоры | 0,26-0,53 |
| Т-клетки с рецептором для ИЛ-2 | 0,01-0,08 |
| Носители маркера апоптоза | 0,11-0,3 |
| Гуморальное звено иммунитета | |
| В-клетки | 0,12-0,33 |
| Иммуноглобулин G | 7,5-15,46 г/л |
| Иммуноглобулин М | 0,65-1,65 г/л |
| Иммуноглобулин A | 1,25-2,52 г/л |
| Иммуноглобулин D | 0-0,07 г/л |
| Неспецифические показатели | |
| Натуральные киллеры | 0,16-0,36 |
| Лимфоциты | 0,17 |
| Моноциты | 0,18 |
| Фагоцитарный показатель | 60-90% |
| Фагоцитарное число | 6-9 единиц |
| РТМЛ со специфическим антигеном | 82-121% |
| РТМЛ с фитогемагглютинином | 21-80% |
| РТМЛ с конкавалином A | 40-76% |
| НСТ-тест спонтанный | 5-12% |
| НСТ-тест активированный | 10-35% |
| Комплемент | 30-50% |
Оценка отклонений от нормы
При расшифровке иммунограммы оценивают уровень отклонения показателей от нормы для дальнейшей регуляции:
- меньше 34% – незначительные нарушения;
- 34-66% – умеренные нарушения, необходима терапия;
- больше 66% – выраженный иммунодефицит.
Ложные показатели анализа крови могут быть вызваны следующими факторами:
- злокачественные опухоли;
- врожденные или хронические аутоиммунные заболевания: ревматоидный артрит, волчанка, склеродермия, васкулит, болезнь Бехтерева;
- вирусные инфекции – ВИЧ, гепатит;
- интоксикация лекарствами или ядами;
- апластическая анемия;
- наличие паразитов в организме;
- последствия радиации.
Когда нарушение иммунитета требует коррекции
Однозначной интерпретации карты анализа не существует. Иммунограмма у детей помогает выявить и исправить иммунологические дефекты, а также может стать основанием для заместительной терапии:
- При недостатке иммуноглобулинов G и М вводят внутривенно препараты из донорской крови.
- При дефектах Т-лимфоцитов применяют препараты из тканей тимуса теленка для дифференцировки и активации клеток.
Для удаления накопившихся иммунных комплексов из крови иногда используется плазмаферез, который сопровождается иммунограммой. Учитывая динамику иммунограммы, можно лечить аллергические и инфекционные заболевания.
Для оценки состояния пациента подсчитывают количество заболеваний за год, учитывая их тяжесть.
Иммунограмма позволяет оценить работу гуморального и клеточного звена, а также эффективность терапии. Для этого используется формула индекса: ((патологический показатель/норма)-1)*100%. В анализе часто учитывают количество В-клеток, цитотоксических форм и Т-хелперов.
Разновидности иммунитета
Медики выделяют два основных типа иммунитета: видовой (наследственный) и индивидуальный (приобретенный).
Видовой иммунитет характерен для всех животных. Он обеспечивает человека защитой от многих заболеваний, присущих другим видам, например, от чумы у собак. В то же время, некоторые болезни человека не опасны для животных. Видовой иммунитет передается генетически от поколения к поколению.
Индивидуальный иммунитет формируется на протяжении жизни и не передается наследникам. Он развивается в ответ на инфекции или интоксикации. Однако некоторые болезни могут ослаблять иммунитет. Например, после гонореи иммунная система может быть ослаблена, что увеличивает риск повторного заражения. В отличие от этого, ветряная оспа обеспечивает стойкий иммунитет, предотвращая повторное заражение на протяжении всей жизни.
Как регулируется иммунный ответ?
Защитная система организма включает множество механизмов контроля и регуляции. Это необходимо для предотвращения аутоиммунных заболеваний и аллергий при слишком сильном иммунном ответе, а также для защиты от инфекций и ядов при слишком слабом ответе.
Регуляция осуществляется на трех уровнях:
- Саморегуляция через взаимодействие иммунных клеток;
- Влияние гормональной системы и печени;
- Воздействие нервной системы.
В иммунной системе действуют специальные Т-хелперы, которые активируют или подавляют производство антител. Также существуют клетки, производящие антиидиотипы — белки, связывающие ранее выработанные антитела. Это необходимо для снижения их концентрации, когда в них больше нет необходимости.
Гормональная система играет важную роль в регуляции иммунного ответа. Почти все гормоны могут усиливать или подавлять иммунные реакции. Например, гормон надпочечников гидрокортизон подавляет иммунный ответ, поэтому препараты на его основе часто применяют для лечения аутоиммунных заболеваний.
Мелатонин, вырабатываемый в шишковидной железе, является примером гормона-стимулятора иммунной системы. Он значительно усиливает иммунитет, хотя механизм его действия до конца не выяснен.
Печень вырабатывает различные иммуносупрессивные соединения и играет ключевую роль в остановке активной фазы иммунного ответа, снижая активность лимфоцитов и макрофагов.
Центральная нервная система также активно регулирует иммунный ответ. За это отвечают участки головного мозга, связанные с лимбической системой и психоэмоциональным состоянием человека. Установлено, что депрессии и другие психические расстройства могут существенно снижать активность защитной системы организма. Механизм регуляции основан на передаче сигналов от нейронов к клеткам иммунной системы.
Параметры регуляции иммунной системы закладываются на генном уровне. У каждого человека формируется индивидуальный набор генов, экспрессия которых в Т-хелперах определяет силу иммунного ответа. Это разнообразие защитных реакций помогает предотвратить распространение инфекций в популяции.
Клетки функциональной системы иммунного гомеостаза.
Иммунокомпетентные клетки:
a) Т-лимфоциты;
b) В-лимфоциты;
c) ЕК.
Антигенпрезентирующие клетки:
a) Макрофаги крови (моноциты) – презентируют антигены, участвуя в гуморальном иммунном ответе через Th2;
b) Нефагоцитирующие А-клетки (клетки Лангерганса, вуалевидные клетки, отростчатые клетки, дендритные клетки, тканевые макрофаги) – играют антигенпрезентирующую роль для клеточного иммунного ответа через Th1, Tctl, ЕК.
Вспомагательные клетки (тучные клетки, базофилы, эозинофилы, тромбоциты) – участвуют в воспалительной реакции.
Иммунокомпетентные клетки (ИКК) подразделяются по функциональной активности на:
Регуляторные ИКК
Эффекторные клетки – непосредственные исполнители иммунного реагирования. Они действуют на объекты либо напрямую, либо через биосинтез биологически активных веществ (иммуноглобулины).
Cluster of differentiation (CD) – маркер, определяющий особенности клеток иммунной системы и обладающий антигенными свойствами.
В 1969 году И. Ройт ввел в иммунологию понятия Т- и В-лимфоцитов:
Т-лимфоциты
В-лимфоциты
Центральной клеткой иммунной системы является лимфоцит (1-4×10^9/л).
Т-лимфоциты – клетки, отвечающие за клеточный иммунитет.
Поверхностные рецепторы Т-лимфоцитов:
— CD2 (рецептор к эритроцитам барана).
— CD3 (рецепторы к антигенам).
— Рецепторы к Fc-фрагменту иммуноглобулинов.
— Рецепторы к белкам системы комплемента (не имеют рецепторов к C3b).
— Рецепторы к интерлейкинам.
Субпопуляции Т-лимфоцитов:
— Нулевые Т-лимфоциты;
— Т-хелперы;
— Эффекторы ГЗТ (ТГЗТ);
— Цитотоксические Т-лимфоциты (Т-киллеры);
— Т-супрессоры;
— Т-клетки памяти.
Т-хелперы первого типа (Th1), выделяющие ИЛ-2, ИЛ-12, ИФН-γ, ФНО-α, обеспечивают реакции Т-клеточного иммунитета.
Т-хелперы второго типа (Th2), секретирующие ИЛ-4, ИЛ-5, ИЛ-10, ИЛ-13, стимулируют синтез антител, т.е. гуморальное звено иммунной системы.
ТГЗТ – эффекторы
Нулевые Т-лимфоциты
Т-хелперы (CD4) распознают антиген в комплексе с антигенами МНС II класса на мембране клеток-мишеней.
Цитотоксические Т-лимфоциты (Т-киллеры, CD8) уничтожают опухолевые клетки, клетки чужеродных трансплантатов, патологически мутированные клетки и клетки, инфицированные вирусами.
Т-супрессоры подавляют активность CD4-лимфоцитов, предотвращая развитие аутоиммунных реакций и защищая организм от нежелательных последствий иммунных реакций. Они также обеспечивают толерантность матери к чужеродным антигенам плода.
Т-клетки иммунологической памяти (CD45RO)
Селекция антител.
Этот процесс определяет, какие антитела должны образоваться для борьбы со специфическим антигеном, выделяя его из миллиардов других потенциально угрожающих организму антигенов. Механизм этой селекции пока не до конца ясен. Логически трудно предположить, что в каждом лимфоците содержится информация для синтеза миллиардов антител, большинство из которых никогда не пригодится. Одна из ранних теорий, известная как «инструктивная», утверждала, что антитела синтезируются в незавершенном виде. Когда антиген попадает в организм, он служит матрицей для окончательного формирования узнающего участка антител, то есть сам антиген является «инструкцией» для создания специфичных к нему антител.
В настоящее время известно, что структура белковой молекулы антитела зависит от последовательности и взаимного расположения аминокислот. Внешние факторы, включая антигены, не вызывают значительных структурных изменений. Поэтому была предложена новая теория — «клональной селекции». Согласно этой теории, в организме человека содержится около 10 миллиардов слегка отличающихся друг от друга лимфоцитов, каждая разновидность которых представлена небольшим количеством клеток. Когда антиген попадает в организм, он связывается только с теми лимфоцитами, которые способны его распознать. Это связывание стимулирует деление клеток, в результате чего образуется большое количество одинаковых клеток — клон, и численность отобранного варианта клеток быстро достигает необходимого уровня.
Теория клональной селекции не объясняла, как возникает колоссальное разнообразие лимфоцитов или их предшественников. Однако недавно механизм этой диверсификации стал более понятным. Показано, что гены клеток, участвующих в иммунной реакции и продукции специфических антител, претерпевают частые случайные изменения за счет перегруппировок отдельных участков. Это приводит к появлению новых клеток с разнообразными признаками, и вся популяция лимфоцитов приобретает способность реагировать на разные антигены. Кроме того, в процессе превращения стволовых клеток в зрелые лимфоциты происходят случайные мутации в генах, кодирующих антитела, что дополнительно увеличивает разнообразие лимфоцитов. Примечательно, что молекулы на поверхности Т-лимфоцитов, отвечающие за их специфичность, имеют схожую структуру с антителами, вырабатываемыми В-лимфоцитами.
Подробнее о В-лимфоцитах
Эти клетки впервые были обнаружены у птиц в органе, известном как Bursa fabricii. Первая буква была добавлена в название лимфоцитов. Они образуются из стволовых клеток в красном костном мозге и выходят оттуда незрелыми. Окончательная дифференциация происходит в селезенке и лимфоузлах, где формируются два типа клеток:
- Плазматические клетки. Это В-лимфоциты, или плазмоциты, которые являются основными «фабриками» по производству антител. Каждый плазмоцит за секунду производит тысячи белковых молекул (иммуноглобулинов), направленных на конкретный вид микроба. Поэтому иммунная система должна дифференцировать множество разновидностей плазматических В-лимфоцитов для борьбы с различными патогенными агентами.
- Клетки памяти. Это малые лимфоциты, которые живут значительно дольше других форм. Они «запоминают» антиген, против которого уже защищали организм. При повторном инфицировании таким агентом они быстро активируют иммунный ответ, вырабатывая большое количество антител. Клетки памяти также присутствуют у Т-лимфоцитов. В этом отношении клеточный и гуморальный иммунитет схожи. Более того, эти два типа защиты от чужеродных агрессоров действуют совместно, так как В-лимфоциты памяти активируются с участием Т-клеток.
Способность запоминать патогенные агенты лежит в основе вакцинации, создающей в организме приобретенный иммунитет. Это умение также проявляется после перенесенных заболеваний, на которые вырабатывается устойчивый иммунитет (например, ветрянка, скарлатина, оспа).
Гуморальный иммунитет
Основное отличие клеточного и гуморального иммунитетов заключается в местонахождении объектов их воздействия. Механизмы защиты от вредоносных агентов также имеют свои особенности. Гуморальный иммунитет в основном обеспечивается В-лимфоцитами. У взрослых они вырабатываются в костном мозге, а у эмбрионов — также в печени. Этот вид защиты называется гуморальным от латинского слова «гумор», что означает «русло». В-лимфоциты вырабатывают антитела, которые отделяются от клеточной поверхности и свободно перемещаются по лимфатическим и кровеносным руслам. Активируют В-лимфоциты чуждые агенты или Т-клетки, что демонстрирует связь и взаимодействие между клеточным и гуморальным иммунитетом.
Особенности барьерной иммунной на разных уровнях
Строение мукозальной иммунной системы в разных частях организма значительно различается из-за специфических условий функционирования органов.
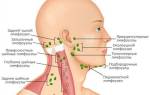
Основой барьерного иммунитета ЛОР-органов и дыхательных путей является глоточное кольцо, состоящее из нескольких скоплений лимфатической ткани:
- Глоточная миндалина;
- Язычная миндалина;
- Трубные миндалины;
- Небные миндалины.
Некоторые из них (небные и язычная) имеют ветвящиеся углубления — крипты, которые увеличивают площадь поверхности миндалин. Крипты являются основным местом взаимодействия иммуноглобулинов и других факторов барьерного иммунитета с микробами. В этих органах также наблюдается высокая концентрация В-лимфоцитов по сравнению с другими лимфоузлами.
Эти клетки вырабатывают IgA и IgG, которые выделяются в пространство крипт и на слизистую оболочку миндалин.
Еще один важный компонент барьерного иммунитета дыхательной системы — эпителиальный слой, содержащий множество иммунных клеток (Т- и В-лимфоциты, макрофаги). Это строение сохраняется до нижних отделов легких, где преобладают М-клетки и клетки, продуцирующие слизь. М-клетки транспортируют антигены в неизменном виде, что позволяет формировать «системный» ответ и способствует устойчивости к многим заболеваниям.
Полость рта выстилает многослойный эпителий, который выделяет большое количество слизи, препятствующей развитию патогенных микробов. Слизь также содержит иммуноглобулины и другие факторы мукозального иммунитета.
Слюнные железы играют важную роль в барьерной системе рта. Слюна содержит высокие концентрации лизоцима, иммуноглобулинов и других веществ, подавляющих развитие патогенных микроорганизмов.
Нарушение состава или выработки слюны является одним из основных факторов, приводящих к кариесу, вызванному условно патогенными микробами, поселяющимися на эмали зуба.
Большую часть кишечника выстилает однослойный ворсинчатый эпителий, включающий слизеобразующие клетки, лимфоциты и М-клетки. В защите кишечника также участвуют лимфатические скопления, такие как:
- Пейеровы бляшки;
- Фолликулы толстой кишки;
- Аппендикс;
- Диффузная лимфоидная ткань в стенках желудка и пищевода.
Симбиотические бактерии, обитающие преимущественно в толстом кишечнике, играют немаловажную роль в иммунной защите. Без них нормальное функционирование пищеварительной системы и мукозального иммунитета было бы невозможным.
Функционирование барьерного иммунитета мочеполовых органов схоже с другими частями этой системы, но имеет ряд особенностей:
- Отсутствие крупных лимфатических скоплений;
- Меньшее количество клеток иммунной системы;
- Преобладание IgG в составе слизи, низкое содержание IgA;
- Высокая концентрация лактобацилл на поверхности эпителия.
На поверхности эпителия влагалища особенно много лактобактерий, которые формируют кислую среду и выделяют антибиотические вещества, препятствующие развитию патогенной микрофлоры.
Основу защитной системы кожи составляет многослойный эпителий, клетки которого, отмирая, формируют практически непроницаемый защитный слой. На его поверхности обитает множество микроорганизмов (более 100 разновидностей), создающих неблагоприятные условия для болезнетворных бактерий.
Дополнительными факторами защиты служат выделения сальных и потовых желез, содержащие лизоцим, иммуноглобулины и другие защитные вещества.
Общая информация
Иммунный ответ — это сложная последовательность биологических процессов в иммунной системе, направленных на реакцию на опасный антиген. Выделяют первичный ответ, который возникает при первом контакте с антигеном, и вторичный, возникающий при повторном контакте.
Первая фаза реакции индуктивна: организм распознает антиген. На клеточном уровне координируются ресурсы, после чего клетки активно размножаются и дифференцируются. Следующий этап начинается, когда клетки иммунного ответа начинают действовать против вредоносных структур. Анализы позволяют оценить результаты иммунного ответа.
Причины ложных результатов
Помимо врожденных особенностей иммунитета, существует множество патологий, которые могут изменить показатели анализа. Важно понимать, что иммунограмма показывает количество и состояние различных групп лейкоцитов и фагоцитов — клеток, отвечающих за защиту организма.
Иммунограмма традиционно используется для выявления наследственных нарушений иммунитета. Перед ее проведением следует исключить распространенные состояния, которые могут негативно влиять на естественную защиту. К ним относятся:
- Злокачественные опухоли;
- Аутоиммунные заболевания: ревматоидный артрит, системные склеродермия и волчанка, различные системные васкулиты (включая болезнь Бехчета, микроскопические и гигантоклеточные васкулиты, узелковый периартериит);
- Вирусные заболевания, включая ВИЧ и гепатиты;
- Выраженные интоксикации: алкоголем, наркотиками, промышленными токсинами, ядами;
- Апластические анемии — болезни, нарушающие рост и созревание клеток крови;
- Последствия радиационного облучения.
Также стоит учитывать, что неправильная подготовка к сдаче крови может привести к ложным результатам. Только после исключения всех перечисленных состояний можно говорить о наличии первичного иммунодефицита. Для подтверждения можно использовать медико-генетическое исследование.
Что такое иммунограмма?
Это специальный анализ крови, который оценивает количество различных иммунных клеток, антител и других веществ, отражающих состояние защитных систем организма. В зависимости от целей исследования и возможностей лаборатории, количество анализируемых параметров может варьироваться. Расширенное исследование охватывает более 25 показателей, позволяя выявить скрытые нарушения, недоступные стандартным методам.
Иммунитет человека делится на два звена: «медленное» (гуморальное) и «быстрое» (клеточное). Быстрое звено реагирует почти сразу после попадания возбудителя (вируса, гриба, бактерии и т. д.) в организм. Основные функции этой группы клеток:
- Поглощение и уничтожение вредоносного агента.
- Презентация информации о патогене другим иммунным клеткам, которые не могут его обнаружить.
- Уничтожение максимального количества выявленных микробов.
- Борьба с опухолями и аутоиммунными процессами, что помогает организму справиться с болезнью.
После поглощения чужеродного тела «быстрым» звеном, начинается медленный процесс создания и выброса антител в кровь. Антитела уничтожают определенные виды патогенных агентов, обладают высокой специфичностью и помогают организму окончательно справиться с заболеванием. Обычно их создание занимает 2-3 недели.
Показатели иммунограммы отражают работу обоих звеньев защиты. На их основе делаются выводы о наличии или отсутствии иммунодефицита, варианте нарушения и оптимальном методе терапии.
| Звено иммунитета, исследуемый параметр | Функция |
|---|---|
| Цитотоксические Т-клетки (CD3+, CD8+) | Распознавание и уничтожение вредоносных микроорганизмов |
| Т-хелперы (CD4+) | Информирование других защитных клеток о наличии патогена, формирование длительного иммунитета |
| Т-супрессоры (CD8+) | Регуляция активности защитных систем, предотвращение аутоиммунных реакций |
| Т-клетки с рецептором для ИЛ-2 (CD25+) | |
| Носители маркера апоптоза (CD95+) | Контроль скорости самоуничтожения клеток |
| В-клетки (CD+, 19CD+) | Выработка специфических антител, защита от повторного заражения |
| Иммуноглобулин G | Антитела, разрушающие стенки вредоносных микробов |
| Иммуноглобулин M | |
| Иммуноглобулин A | |
| Иммуноглобулин E | Участие в аллергических реакциях |
| Натуральные киллеры (CD16+) | Обеспечение противоопухолевого иммунитета |
| Клетки с HLA маркером | Отражение активности иммунных механизмов |
| Фагоцитоз | Распознавание и поглощение вредоносных агентов |
| Реакция торможения миграции лейкоцитов (РТМЛ) | Тест, отражающий работу клеточного звена |
| НСТ-тест | Оценка активности фагоцитоза |
| Комплемент | Предотвращение формирования крупных иммунных комплексов, участие в нейтрализации микробов |
В некоторых случаях врач может рекомендовать исследование содержания интерлейкинов в крови. Эти вещества обеспечивают взаимосвязь различных компонентов защитных систем, и их нарушение может привести к иммунодефицитным состояниям.
Т-клетки и что о них нужно знать
Из школьной программы многие помнят, что за иммунитет отвечают лимфоциты. Существует два типа лимфоцитов: В-клетки, которые образуются и созревают в костном мозге, и Т-клетки, образующиеся в костном мозге и созревающие в вилочковой железе (тимусе) в верхней части грудной клетки. В организме они работают вместе, но Т-клетки играют более важную роль.
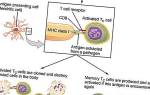
Т-клетки нацелены на выявление и устранение специфических инородных частиц. Вместо того чтобы атаковать все антигены подряд (бактерии, вирусы, токсины и даже пыльцу), Т-клетки циркулируют до тех пор, пока не встретят «свой» антиген. Они распознают его с помощью белков на поверхности, которые связываются с белками антигенов. Существуют триллионы вариантов этих белков, каждый из которых может распознать свою мишень.
Роль Т-клеток меняется на протяжении жизни. В детстве они помогают формировать иммунитет к общим патогенам и создают запас Т-клеток памяти. Эти клетки запоминают реакцию на определенные антигены, поэтому при повторной встрече реагируют быстрее и эффективнее (это называется вторичным иммунным ответом). В дальнейшем Т-клетки в основном занимаются иммунорегуляцией и работают с повторяющимися или постоянно присутствующими антигенами (например, при хронических заболеваниях). С возрастом их количество снижается, и иммунитет ослабевает.
Т-клетки также бывают разных типов. Т-хелперы помогают другим иммунным клеткам, высвобождая цитокины, которые стимулируют созревание В-клеток для выработки антител против патогенов. Т-киллеры (цитотоксические T-лимфоциты) убивают поврежденные или инфицированные клетки организма.
Виды иммунного ответа
Все иммунные реакции делятся на две категории:
- Врожденные;
- Приобретенные.
Врожденный ответ основан на генетически закодированных механизмах защиты организма от патогенов. Это древнейшая система иммунитета, присутствующая практически у всех живых организмов. Она характеризуется быстрой реакцией и высокой эффективностью: токсин или микроб уничтожается за считанные часы, что предотвращает развитие заболевания.
Некоторые исследователи также относят противораковую активность иммунной системы к этой категории. Однако механизмы противоопухолевых реакций еще не полностью изучены, и возможно, их выделят в отдельную категорию иммунного ответа.
Приобретенный иммунный ответ возникает при первом контакте организма с патогенами. Он проявляется разнообразными симптомами, такими как кашель, насморк и повышение температуры тела во время простуды. Эти симптомы отражают сложные процессы в иммунной системе, направленные на уничтожение возбудителя.
Приобретенный иммунный ответ лежит в основе действия всех вакцин и естественного выздоровления от инфекционных заболеваний, отравлений токсинами и ядами животных.
Иммунный ответ также делится на клеточный и гуморальный. Это деление условно, так как в организме трудно отделить клеточные реакции от гуморальных — они тесно взаимосвязаны. Тем не менее, такое разделение помогает упростить понимание этих сложных процессов.
Оценка иммунного статуса
Иммунный статус (расширенный) — это количественная и качественная характеристика работы различных органов иммунной системы и механизмов защиты.
Иммунограмма — метод изучения иммунного статуса, основанный на анализе крови для определения состояния основных показателей иммунитета.
Ключевые показатели состояния иммунной системы — иммуноглобулины:
- IgA — защищают слизистые оболочки и противостоят токсинам;
- IgM — первыми реагируют на патогенные микроорганизмы, их уровень указывает на острое воспаление;
- IgG — повышенный уровень свидетельствует о хроническом воспалительном процессе, так как они появляются позже после воздействия раздражителя;
- IgE — участвуют в аллергических реакциях.
Оценка иммунологического статуса может проводиться в один или два этапа. Скрининговый тест включает определение количественных показателей сыворотки крови, уровней иммуноглобулинов и аллергологических проб.
Расширенные методы оценки включают изучение фагоцитарной активности нейтрофилов, Т-клеток, В-клеток и системы комплемента. На первом этапе выявляются дефекты иммунной системы, на втором — проводится подробный анализ. Время исследования зависит от клиники и метода диагностики (скрининговый тест или расширенная иммунограмма) и составляет в среднем 5-15 дней.
Первый этап — ориентировочный уровень, включает следующие тесты:
- Фагоцитарные показатели — количество нейтрофилов и моноцитов, реакция фагоцитов на микробы.
- Т-система — количество лимфоцитов и соотношение зрелых клеток и субпопуляций.
- В-система — концентрация иммуноглобулинов, соотношение процента и абсолютного числа В-лимфоцитов в периферической крови.
Второй этап — аналитический уровень, включает:
- Фагоцитарная функция — активность хемотаксиса и экспрессия молекул адгезии.
- Анализ Т-системы — продукция цитокинов, активность лимфоцитов, выявление молекул адгезии и аллергическая реакция.
- Анализ В-системы — исследование иммуноглобулинов IgG и секреторного субкласса IgA.
Формы иммунного ответа.
Иммунный ответ — это последовательность сложных процессов в иммунной системе, возникающих в ответ на антиген.
Различают:
1) первичный иммунный ответ (при первой встрече с антигеном);
2) вторичный иммунный ответ (при повторной встрече с антигеном).
Иммунный ответ состоит из двух фаз:
1) индуктивной — представление и распознавание антигена, сопровождающееся кооперацией клеток, пролиферацией и дифференцировкой;
2) продуктивной — обнаружение продуктов иммунного ответа.
При первичном иммунном ответе индуктивная фаза может длиться до недели, а при вторичном — до 3 дней благодаря клеткам памяти.
Антигены, попадая в организм, взаимодействуют с антигенпредставляющими клетками (макрофагами), которые экспрессируют антигенные детерминанты на своей поверхности и передают информацию об антигене в периферические органы иммунной системы, где происходит активация Т-хелперов.
Иммунный ответ может проявляться в одном из трех вариантов:
1) клеточный иммунный ответ;
2) гуморальный иммунный ответ;
3) иммунологическая толерантность.
Клеточный иммунный ответ осуществляется Т-лимфоцитами. Образуются эффекторные клетки — Т-киллеры, которые уничтожают клетки с антигенной структурой через прямую цитотоксичность и синтез лимфокинов, участвующих во взаимодействии клеток (макрофагов, Т- и В-клеток). В регуляции иммунного ответа участвуют два подтипа Т-клеток: Т-хелперы усиливают ответ, Т-супрессоры подавляют его.
Гуморальный иммунитет обеспечивается В-клетками. Т-хелперы передают антигенную информацию В-лимфоцитам, которые формируют клон антителопродуцирующих клеток. В-клетки преобразуются в плазматические клетки, секретирующие иммуноглобулины (антитела) с высокой специфичностью к антигену.
Антитела взаимодействуют с антигеном, образуя комплекс АГ-АТ, который активирует неспецифические защитные механизмы. Эти комплексы активируют систему комплемента. Взаимодействие комплекса АГ-АТ с тучными клетками вызывает дегрануляцию и выделение медиаторов воспаления — гистамина и серотонина.
При низкой дозе антигена развивается иммунологическая толерантность: антиген распознается, но не вызывает продукции клеток и гуморального иммунного ответа.
Иммунный ответ характеризуется:
1) специфичностью (реакция направлена только на определенный антиген);
2) потенцированием (усиленный ответ при повторном поступлении одного и того же антигена);
3) иммунологической памятью (способность распознавать и усиливать ответ на тот же антиген при повторном попадании, даже через длительные промежутки времени).