Симптомы Хронического миелоидного лейкоза:
Момент возникновения хронического миелоидного лейкоза (ХМЛ), как и других лейкозов, не имеет симптомов и проходит незамеченным. Симптоматика развивается, когда общее количество опухолевых клеток превышает 1 килограмм. Большинство пациентов жалуются на общее недомогание, быструю утомляемость и одышку при физической нагрузке. Из-за анемии кожа становится бледной. Пациенты могут испытывать дискомфорт в левой половине живота из-за увеличения селезенки. Часто наблюдаются потеря веса, усиленная потливость и непереносимость жары. При клиническом осмотре чаще всего единственным патологическим признаком является увеличение селезенки. Увеличение печени и лимфатических узлов на ранних стадиях ХМЛ встречается редко. Примерно у четверти пациентов заболевание обнаруживается случайно во время планового обследования. Иногда диагноз ставится на более агрессивной стадии — акселерации или бластного криза.
Хронический миелоидный лейкоз протекает в две стадии:
- Первая стадия — доброкачественная, длится несколько лет и характеризуется увеличением селезенки.
- Вторая стадия — злокачественная, длится 3-6 месяцев. Увеличиваются селезенка, печень и лимфатические узлы, появляются лейкозные инфильтрации кожи, нервных стволов и мозговых оболочек. Развивается геморрагический синдром.
Часто регистрируются инфекционные заболевания. Признаки интоксикации включают слабость и потливость. Иногда первым симптомом является боль или тяжесть в левом подреберье, связанная с увеличением селезенки, что может привести к инфарктам селезенки. Без видимой причины может подниматься температура и возникать боль в костях.
В типичном случае наблюдается нейтрофильный лейкоцитоз с появлением молодых форм нейтрофилов, увеличением тромбоцитов и уменьшением лимфоцитов. По мере прогрессирования болезни нарастают анемия и тромбоцитопения. У детей чаще встречается ювенильная форма ХМЛ без увеличения тромбоцитов, но с повышенным содержанием моноцитов. Часто увеличивается число базофилов и уровень эозинофилов. В первой стадии клетки костного мозга соответствуют норме. Во второй стадии в костном мозге и крови появляются бластные формы, наблюдается быстрый рост числа лейкоцитов (до нескольких миллионов в 1 мкл). В конечной стадии в крови обнаруживаются осколки ядер мегакариоцитов, угнетается нормальное кроветворение.
Болезнь протекает хронически с периодами обострения и ремиссии. Средняя продолжительность жизни составляет 3-5 лет, но известны случаи длительного течения (до 10-20 лет). Клиническая картина зависит от стадии заболевания.
Прогноз неоднозначен и зависит от стадии. В течение первых двух лет после диагноза умирает 10% больных, каждый последующий год — чуть меньше 20%. Медиана выживаемости составляет около 4 лет.
Для определения стадии заболевания и риска летального исхода используют прогностические модели, основанные на многофакторном анализе ключевых признаков. Одна из них — индекс Сокала, учитывающий процент бластных клеток в крови, размеры селезенки, число тромбоцитов, дополнительные цитогенетические нарушения и возраст. Модели Тура и комбинированная модель Кантарджана учитывают количество неблагоприятных прогностических признаков. К ним относятся: возраст 60 лет и старше; значительная спленомегалия (нижний полюс селезенки выступает из левого подреберья на 10 см или более); содержание бластных клеток в крови или костном мозге, равное или превышающее 3% и 5% соответственно; содержание базофилов в крови или костном мозге, равное или превышающее 7% и 3% соответственно; уровень тромбоцитов, равный или превышающий 700000 1/мкл, а также все признаки стадии ускорения. При наличии этих признаков прогноз крайне неблагоприятный; риск летального исхода в течение первого года заболевания втрое выше обычного.
Клинические проявления заболевания
При развитии острого миелоидного лейкоза (ОМЛ) наблюдаются следующие синдромы:
- гиперпластический;
- геморрагический;
- анемический;
- интоксикация и нейролейкоз;
- лейкостазы.
Эти синдромы проявляются типичной симптоматикой, указывающей на системное поражение организма. Общие признаки заболевания включают постоянную усталость, плохой аппетит и бледность кожи. Возможны спонтанные повышения температуры, которые иногда принимают за простуду. На начальных стадиях увеличения лимфоузлов не наблюдается. Иногда возникают болезненные ощущения в ногах при ходьбе, которые вскоре проходят. ОМЛ развивается постепенно, поэтому его симптомы появляются не сразу. Распознать заболевание на ранней стадии можно по развернутому анализу крови. Многие пациенты не подозревают о наличии болезни, а тревожные симптомы списывают на усталость и переутомление.
На поздних стадиях ОМЛ возникают тяжелая интоксикация, лейкостазы и нейролейкоз.
Гиперпластический синдром
Когда недозрелые клетки попадают в кровь, в органах человека возникает инфильтрация тканей. У больного наблюдаются следующие признаки:
- увеличение периферических лимфоузлов и нёбных миндалин;
- увеличение селезёнки (спленомегалия);
- ощущение тяжести в области печени и её увеличение;
- отёчность верхних и нижних конечностей, лица;
- боли в мышцах, костях и суставах.
Отёки возникают из-за разрастания средостенных лимфатических узлов. Увеличенные лимфоузлы сдавливают верхнюю полую вену, что нарушает кровообращение. В результате отекает шея, лицо приобретает синеватый оттенок, и больному трудно дышать. В тяжёлых случаях развивается стоматит Венсана, проявляющийся отёчностью дёсен, болью и трудностями при приёме пищи.
Геморрагический синдром
Незрелые миелобласты препятствуют выработке других кровяных клеток, включая тромбоциты, что приводит к геморрагическому синдрому. Он проявляется следующими симптомами:
- истончение стенок сосудов;
- кровотечения из носа и под кожей, образование множественных гематом;
- длительное кровотечение, трудное для остановки;
- постоянное кровотечение из дёсен.
Гематомы могут возникать даже при незначительном надавливании на кожу. При геморрагическом синдроме существует высокий риск кровоизлияния в мозг.
Анемический синдром
Для анемического синдрома характерны:
- сильная слабость;
- бледность кожи;
- апатия;
- беспричинные головные боли;
- обмороки;
- головокружение;
- боли в сердце;
- желание есть мел.
Анемические проявления легко спутать с обычным недомоганием. Выпадение волос и ломкость ногтей пациенты часто связывают с нехваткой витаминов. Если состояние не улучшается, необходимо пройти обследование, чтобы исключить злокачественные заболевания крови.
Интоксикация и нейролейкоз
При интоксикации наблюдаются:
- быстрая потеря веса;
- снижение аппетита;
- обильное потоотделение;
- высокая температура (37-40°C);
- тошнота и рвота;
- понос.
На поздней стадии острого миелоидного лейкоза (ОМЛ) из-за снижения иммунитета могут развиваться бронхиты, воспаления легких и тяжелые грибковые инфекции слизистых.
Нейролейкоз — это комплекс симптомов, возникающих при поражении мозга. Пациента беспокоят сильные головные боли, тошнота и рвота. Возможны приступы, напоминающие эпилептические. При обследовании выявляется стойкое повышение внутричерепного давления. У больного ухудшается слух, нарушается речь, снижается острота зрения. При системном поражении мозговых структур возникают сумеречные состояния и нарушения восприятия окружающего мира.
Лейкостазы
При остром миелобластном лейкозе общее замедление кровотока (лейкостаз) указывает на неблагоприятный прогноз. Число незрелых клеток в крови превышает 100 000 1/мкл, что приводит к повышенной вязкости крови и застою в органах. Из-за истончения сосудов риск геморрагического инсульта значительно возрастает, а летальность при лейкостазах высока.
Если лейкостаз возникает в малом круге кровообращения, это может вызвать проблемы с дыханием и двустороннюю пневмонию. Лечение пневмонии затруднено, так как иммунная система пациента подавлена, а уровень кислорода в крови снижается. Инфекционные заболевания на поздней стадии ОМЛ протекают тяжело и могут привести к серьезным осложнениям.
Можно ли прогнозировать исход болезни?
Прогноз зависит от стадии заболевания, его формы и реакции пациента на лечение. При острых миелолейкозах пятилетняя выживаемость достигается у 15–70% пролеченных пациентов, а ремиссия наблюдается у 30–78% больных.
При хронической форме наилучшие результаты достигаются при начале лечения на ранней стадии (почти 85%). Если заболевание прогрессирует, в течение первых двух лет погибает 10% пациентов, а с третьего года — по 15% ежегодно.
Существуют модели прогнозирования летального исхода, учитывающие неблагоприятные факторы, такие как:
- возраст;
- размеры селезенки;
- доля бластных клеток в крови;
- количество тромбоцитов и базофилов.
Хронические формы заболевания дают больше шансов на выздоровление, чем острые. Поэтому важно начинать лечение незамедлительно, не затягивать с диагностикой и следовать рекомендациям врачей.
Научные исследования ежегодно приносят новые достижения в терапии. Необходимо настраивать пациента на достижение ремиссии и последующее наблюдение.
Исследования при лейкозах
Диагностика лейкозов включает анализ крови и костного мозга. Точный диагноз ставится после биопсии из бедра или ребра.
Сначала проводят анализ крови, где наблюдаются отклонения в показателях лейкоцитов. Результаты могут варьироваться от 0,110^9/л до 1010^9/л. Небольшие изменения могут указывать на монобластную лейкемию или эритромиелоз. В сыворотке крови базофилы отсутствуют, а скорость оседания эритроцитов (СОЭ) повышена.
Эритроциты имеют низкие показатели, в крови преобладают бласты и клетки зернистого ряда, также отмечаются созревшие моноциты. Уровень гемоглобина снижен.
Биохимическое исследование определяет уровень общего белка, билирубина, альбумина, мочевины и креатинина.
Для острого лейкоза первой фазы анализ крови может показать:
- Общий белок – 78 ммоль/л.
- Общий билирубин – 14-17 ммоль/л.
- Прямой билирубин – 3,5-4,5 ммоль/л.
- Креатинин – 108 мкмоль/л.
Цитохимические показатели позволяют изучить активность ферментов и состав крови, костного мозга и других тканей.
Иммунологический тест исследует нарушения в работе иммунной системы, используя венозную кровь для определения иммунных клеток, их функций и способности уничтожать бактерии.
Для выявления метастазов в миокарде применяются электрокардиограмма и эхокардиография.
Ультразвуковая диагностика позволяет выявить отклонения во внутренних органах, включая печень, органы ЖКТ и мочеполовой системы, а также лимфатические узлы.
Глобальная диагностика всех органов и систем осуществляется с помощью магнитно-резонансной и компьютерной томографии, которые послойно сканируют тело и выявляют даже незначительные изменения в тканях.
Лечение
При хроническом миелолейкозе лечение зависит от стадии опухолевых клеток. При слабовыраженных клинико-гематологических проявлениях в хронической стадии рекомендуется полноценное питание с витаминами, регулярное диспансерное наблюдение и общеукрепляющая терапия. Положительное влияние на течение заболевания может оказать «Интерферон».
При лейкоцитозе назначают «Миелосан» в дозе 2-4 мг/сутки. При более высоком лейкоцитозе дозу увеличивают до 6-8 мг/сут. Цитопенический эффект проявляется не ранее чем через 10 дней после начала лечения. Уменьшение размеров селезенки и цитопенический эффект наблюдаются в среднем через 3-6 недель при общей дозе от 200 до 300 мг. Далее терапия продолжается с приемом 2-4 мг «Миелосана» раз в неделю для поддержания эффекта. При первых признаках обострения проводится миелосанотерапия.
Лучевая терапия может применяться при спленомегалии. Для пациентов с прогрессирующей стадией болезни актуальны поли- и монохимиотерапия. При значительном лейкоцитозе и недостаточной эффективности «Миелосана» назначается «Миелобромол» (125-250 мг в день) с контролем показателей периферической крови.
При значительной спленомегалии назначают «Допан» (6-10 г/сутки) на 4-10 дней. Интервалы между приемами зависят от уменьшения числа лейкоцитов и размеров селезенки. Как только уровень лейкоцитов становится приемлемым, прием «Допана» прекращается.
Если развивается резистентность к «Допану», «Миелосану», лучевой терапии и «Миелобромолу», назначается «Гексафосфамид». В прогрессирующей стадии используются программы ЦВАМП и АВАМП.
При резистентности к цитостатической терапии лечение ориентируется на лейкоцитофарез в сочетании с полихимиотерапией. Срочными показаниями к лейкоцитофарезу являются клинические признаки стаза в сосудах головного мозга (тяжесть в голове, снижение слуха, головные боли) из-за гипертромбоцитоза и гиперлейкоцитоза.
При бластном кризе применяются различные программы химиотерапии, а трансфузии эритроцитарной массы, тромбоконцентрата и антибактериальная терапия показаны при инфекционных осложнениях, анемии и тромбоцитопенической геморрагии.
На хронической стадии миелолейкоза эффективна трансплантация костного мозга, обеспечивающая клинико-гематологическую ремиссию в 70 % случаев.
Срочным показанием для спленэктомии является угроза разрыва или сам разрыв селезенки, а относительными показаниями — тяжелый абдоминальный дискомфорт.
Пациентам с экстрамедуллярными опухолевыми образованиями, угрожающими жизни, показана лучевая терапия.
Хотите получить смету на лечение?
Точный расчет сметы на лечение возможен только при наличии данных о заболевании пациента.
Особенности питания
Несмотря на ухудшение аппетита при хроническом и остром миелоидном лейкозе, важно следовать предписанному специалистом режиму питания.
Для восстановления сил и удовлетворения потребностей организма, пострадавшего от миелобластного лейкоза, а также для предотвращения негативных последствий интенсивной терапии необходима сбалансированная диета.
Рекомендуется дополнять рацион следующими продуктами:
- Продукты, богатые витамином C и микроэлементами.
- Зелень, овощи, ягоды.
- Рисовая, гречневая и пшеничная каши.
- Морская рыба.
- Нежирные молочные продукты (пастеризованное молоко, творог).
- Мясо кролика и субпродукты (почки, язык, печень).
- Прополис и мед.
- Травяной и зеленый чай (обладают антиоксидантным действием).
- Оливковое масло.
Для предотвращения перегрузок пищеварительного тракта и других систем при миелолейкозе из меню исключают:
- Алкоголь.
- Продукты с трансжирами.
- Фастфуд.
- Копченые, жареные и соленые блюда.
- Кофе.
- Сдобу и кондитерские изделия.
- Продукты, разжижающие кровь (лимон, калина, клюква, какао, чеснок, орегано, имбирь, паприка, карри).
При миелолейкозе важно контролировать объем потребления белковой пищи (не более 2 г на 1 кг массы тела в сутки) и поддерживать водный баланс (от 2 до 2,5 л жидкости в сутки).
Миелолейкоз причины
Этиология миелолейкоза до сих пор не выяснена. Предполагается, что в развитии как острой, так и хронической формы миелолейкоза важную роль играют нарушения в структуре и составе хромосом, которые могут быть как наследственными, так и приобретёнными под воздействием мутагенных факторов.
К причинам миелолейкоза относятся химические канцерогены. Доказано, что острые миелолейкозы чаще встречаются у людей, подвергавшихся воздействию бензола или принимавших цитостатические препараты (например, Имуран, Мустарген, Саркозолин, Лейкеран, Циклофосфан). Частота заболевания среди таких пациентов увеличивается в несколько раз. Известны случаи, когда миелолейкоз развивался на фоне длительного лечения других онкологических заболеваний с применением лучевой терапии. Таким образом, ионизирующая радиация считается одним из предрасполагающих факторов.
Миелолейкоз может развиваться из-за не врождённого повреждения хромосом в единственной стволовой клетке. Причины таких изменений пока неизвестны. Возможно, происходят случайные обмены на генетическом уровне между хромосомами, расположенными близко друг к другу на определённом этапе жизни клетки. Анализ хромосом показывает, что при миелолейкозе в организме распространяются клональные опухолевые лейкозные клетки — потомки одной клетки, изначально подвергшейся мутациям. Нестабильный генотип патологических клеток способствует образованию новых клонов, а также под воздействием медицинских препаратов происходит отбор наиболее автономных клонов. Этот феномен указывает на прогрессирующее течение миелолейкоза и его уход от контроля со стороны цитостатических препаратов.
Также рассматривается возможность участия некоторых вирусов в возникновении заболевания.
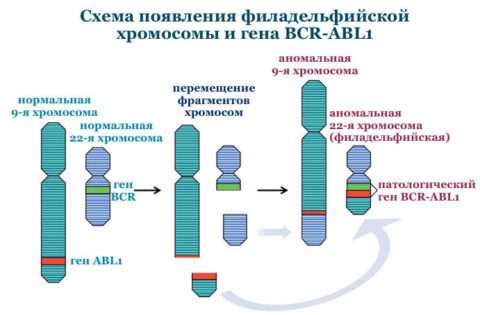
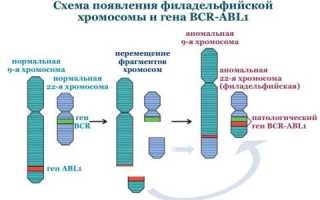
Патогенез хронического миелолейкоза
Патогенез хронического миелолейкоза
Гибридный ген BCR-ABL1, образующийся в результате транслокации хромосом, синтезирует белок BCR-ABL. Этот белок представляет собой тирозинкиназу, которая обычно передает сигналы для роста клеток. Однако мутировавшая тирозинкиназа становится активным фактором пролиферации, что приводит к бесконтрольному делению клеток независимо от факторов роста и образованию клонов мутировавших клеток.
Бесконтрольное деление клеток нарушает апоптоз — запрограммированную гибель клеток. Кроме того, гибридная тирозинкиназа подавляет функции восстановления ДНК, что создает предпосылки для новых мутаций и усугубляет патологический процесс.
Размножающиеся клетки являются незрелыми, бластными предшественниками полноценной крови. Постепенно бластные клетки вытесняют функциональные эритроциты, тромбоциты и лейкоциты. Также происходят изменения в других хромосомах, что ускоряет разрушение организма в целом.
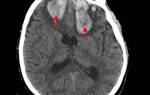
Диагностика заболевания
- Исследование крови. Позволяет выявить показатели и соотношение клеток крови. При развитии заболевания увеличивается количество незрелых белых клеток, а по мере ухудшения состояния снижается уровень тромбоцитов и эритроцитов.
- Биохимическое исследование крови. Методика помогает выявить нарушения в работе селезенки и печени, возникающие из-за проникновения незрелых лейкоцитов.
- Цитогенетический анализ. Исследование хромосом позволяет обнаружить аномальную филадельфийскую хромосому в лейкозных клетках при развитии заболевания.
- Аспирация и биопсия костного мозга. Эти процедуры обеспечивают получение максимальной информации и обычно выполняются одновременно, с забором материала из задней области бедренной кости.
- Гибридизация для определения аномальных хромосом.
- МРТ и КТ.
- Ультразвуковое исследование.
Первичные признаки хронического миелолейкоза выявляются при анализе крови, где наблюдается высокий уровень гранулоцитов. Это требует дополнительных исследований и дифференциальной диагностики, включая гистологическое исследование.
Как проявляется миелолейкоз?
Поражая кроветворные ростки, болезнь проходит через развернутую и терминальную стадии. На начальном этапе могут отсутствовать клинические проявления. Лабораторно в крови выявляется лишь лейкоцитоз и появление юных форм клеток. Также обнаруживается филадельфийская хромосома и дисбаланс между эритроцитами и лейкоцитами в костном мозге.
Эта стадия может длиться около четырех лет. При ранней диагностике и начале лечения человек долгое время не ощущает симптомов.
На терминальной стадии больной жалуется на гипертермию, резкое снижение массы тела, выраженную слабость и боль в костях. При пальпации увеличиваются размеры селезенки и печени.
При диагностике отмечается повышенное количество бластов и угнетение кроветворных ростков, что приводит к снижению уровня лейкоцитов, тромбоцитов и эритроцитов.
Миелолейкоз имеет несколько стадий:
-
Хроническая фаза — длится до трех лет, в течение которых симптомы могут отсутствовать. Постепенно увеличиваются селезенка, уровень лейкоцитов и тромбоцитов. После трех лет появляются слабость, потливость и дискомфорт в левом подреберье.
-
Стадия акселерации — клинически не отличается от хронической, но лабораторно выявляется повышение базофилов и наличие миелоцитов, метамиелоцитов, промиелоцитов и бластных клеток. Возможны зуд, диарея и чувство жара. Если после курса химиотерапии количество базофилов не снижается, это указывает на неблагоприятный прогноз и прогрессирование терминальной фазы.
-
Терминальная стадия — характеризуется резкой слабостью, суставной и костной болью, лихорадкой до 39 градусов, ознобом, снижением массы тела, спленомегалией и гепатомегалией. Среди осложнений — инфаркт селезенки, проявляющийся острой болью в левом подреберье, иррадиирующей в спину, и гипертермией до 38 градусов.
Симптомы на последней стадии связаны с изменениями в крови. Снижение лейкоцитов приводит к нарушению работы иммунной системы, обострению хронических заболеваний, прогрессированию инфекций и воспалению лимфоузлов.
Тромбоцитопения вызывает нарушения свертываемости и развитие геморрагического синдрома. На коже и слизистых могут появляться сыпь, увеличивается время кровоточивости при ранах или менструации. При анемии возможны головокружения, слабость, бледность и потеря сознания из-за недостатка питательных веществ и кислорода в органах, включая головной мозг.
Острый миелолейкоз в начале проявляется симптомами, похожими на грипп: ломота в суставах, субфебрилитет, снижение аппетита, слабость и одышка. Эта форма быстро прогрессирует и часто приводит к летальному исходу (15-70%) несмотря на лечение.
Открыть XML через блокнот
Операционная система Windows в предустановленном состоянии может взаимодействовать с файлами большинства текстовых форматов. Хотя некоторые символы могут отображаться некорректно из-за кодировки, основную суть текста обычно уловить несложно. Главное — проявить терпение и попробовать разные настройки. Вот инструкция:
-
Сначала загрузите нужный файл на компьютер в любую папку. Затем можно открыть «Блокнот», введя его название в поиске меню «Пуск», или перейти в каталог, куда был загружен XML-документ, и вызвать меню взаимодействия для выбора нужного действия.
-
В результате документ откроется в исходном виде с тегами, атрибутами и описанием действий. Это может быть не слишком информативно для большинства пользователей, поэтому стоит искать альтернативные источники для более удобного восприятия информации.
Лечебная тактика
Лечение проводится в стационаре, что снижает контакт с окружающим миром. Клинические рекомендации включают химиотерапию, которую онкогематолог подбирает индивидуально. При диагнозе «Острый миелобластный лейкоз» врачи назначают комбинацию препаратов. Интенсивная химиотерапия способствует выздоровлению и достижению стойкой ремиссии.
На первом этапе лечения препараты уничтожают как раковые, так и здоровые клетки, что вызывает побочные эффекты:
- Тошнота;
- Рвота;
- Вялость;
- Язвенные поражения полости рта;
- Назальные кровотечения;
- Повышенный риск инфекций.
На втором этапе назначают несколько курсов цитостатиков. Для уничтожения раковых клеток важен прием высокой дозы цитозин-арабинозида, который препятствует образованию частиц, переносящих наследственную информацию. При печеночной и почечной недостаточности или угнетении костного мозга прием препарата противопоказан.
Для угнетения функций костного мозга и борьбы с опухолевыми клетками назначают Идарубицин. Митоксантрон подавляет иммунитет и уничтожает опухоли. Для максимальной эффективности применяются протоколы с тремя блоками постремиссионной химиотерапии. Прогноз жизни на фоне химиопрепаратов значительно улучшается.
При поражении центральной нервной системы рекомендована лучевая терапия. Ионизирующее излучение воздействует на аномальные клетки, нарушая их структуру и вызывая гибель.
Полное выздоровление возможно после пересадки костного мозга. Этот метод имеет свои нюансы и последствия:
- Перед операцией (вливание донорского материала через катетер в артерию) больному уничтожают костный мозг высокими дозами химиотерапии.
- При отсутствии иммунитета любые инфекции, например, ОРЗ или даже царапина, могут привести к летальному исходу.
- Трансплантируемый материал может не взаимодействовать с организмом пациента:
- Если организм воспринимает чужой костный мозг как чужеродный, он отторгает его, что нарушает работу всех органов. Иммунные клетки уничтожают все на своем пути, но при этом окончательно уничтожаются раковые клетки. Иммуносупрессивная терапия помогает восстановить нормальный кроветворный процесс.
- Если организм отвергает введенные стволовые клетки, иммунитет не формируется, и выработка кровяных телец не начинается.
- При введении биоматериала возможны аллергические реакции или анафилактический шок.
- Половина пациентов умирает в первый месяц после операции.
Найти подходящий костный мозг сложно. Лучшие доноры — однояйцевые близнецы, родные братья и сестры. Материал родителей подходит крайне редко. Стволовые клетки могут быть взяты у самого пациента в период ремиссии или у постороннего человека.