Миеломная болезнь крови, или множественная миелома, — это злокачественное заболевание, при котором происходит аномальное разрастание плазматических клеток в костном мозге. Это приводит к образованию опухолей и нарушению кроветворения. В статье рассмотрим механизм развития миеломы, основные симптомы, классификацию по стадиям, а также методы лабораторной и инструментальной диагностики. Понимание этих аспектов важно для своевременного выявления заболевания и выбора эффективных методов лечения, что может улучшить качество жизни пациентов и повысить шансы на выздоровление.
Механизм зарождения и развития
Причины, вызывающие развитие заболевания, остаются неясными. Однако существует информация о том, что ионизирующая радиация может способствовать увеличению его распространенности.
Патологический процесс начинается с трансформации полипотентной стволовой клетки в опухолевую. При этом фиксируются многочисленные хромосомные аномалии. Тем не менее, болезнь может не проявлять себя на протяжении 20-30 лет, что делает случаи её диагностики до 40 лет довольно редкими.
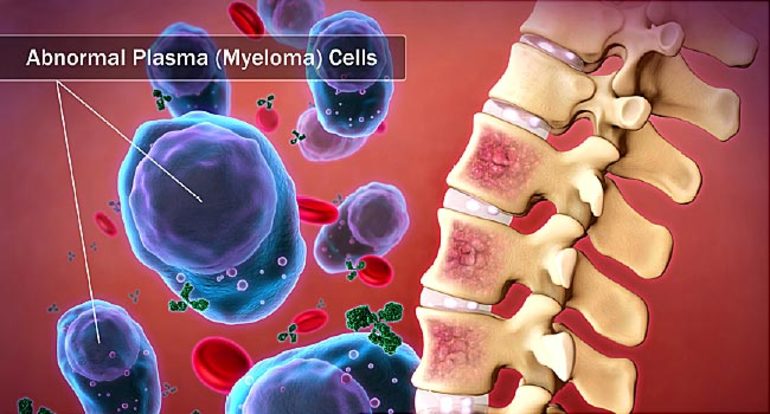
За этот период клетка, получившая новые свойства, проникает в костную ткань и почки, формируя многоочаговую опухоль. Чаще всего она локализуется в позвоночнике и плоских костях черепа, рёбер и таза, что приводит к остеолизу и остеопорозу. Кальций, высвобождающийся из разрушенных костей, попадает в кровь и оседает в виде плотных образований в органах выделения — почках, лёгких и слизистой желудка.
https://youtube.com/watch?v=j4P0DcvnYPY
Миеломная болезнь крови представляет собой сложное заболевание, которое требует внимательного анализа и глубокого понимания. Врачи отмечают, что это злокачественное новообразование, возникающее из плазматических клеток, может проявляться разнообразными симптомами, включая анемию, боли в костях и повышенную предрасположенность к инфекциям. Специалисты подчеркивают важность ранней диагностики, так как это существенно влияет на эффективность лечения. Современные методы терапии, такие как химиотерапия и иммунотерапия, показывают обнадеживающие результаты, однако врачи предупреждают о необходимости индивидуального подхода к каждому пациенту. Регулярное наблюдение и контроль состояния здоровья играют ключевую роль в управлении заболеванием и повышении качества жизни пациентов.
Классификация по стадиям
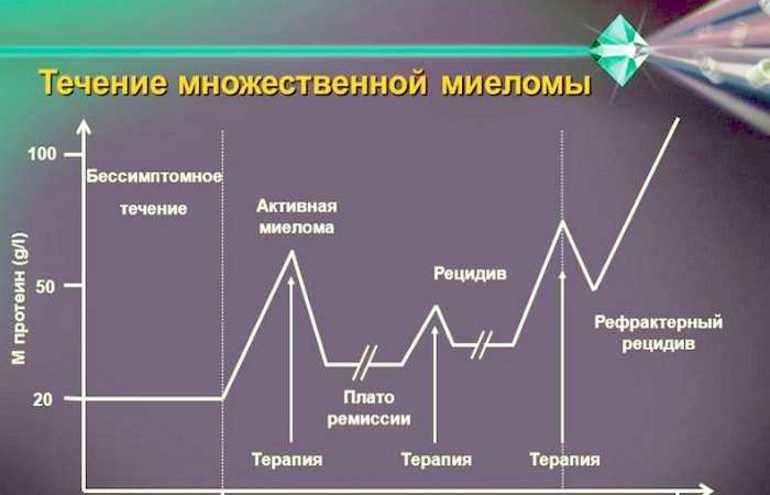
Миеломная болезнь проходит через несколько этапов своего развития, в течение которых опухоль увеличивает свою массу. Определить эти стадии можно следующим образом:
- I стадия (низкая масса). Уровень гемоглобина в эритроцитах превышает 100 г/л. Парапротеин класса lgG составляет менее 5%, или иммуноглобулин класса lgA — менее 3%. Концентрация бета-2-микроглобулина не превышает 3,5 мг/л, а уровень альбумина составляет 3,5 г/дл или более. Уровень кальция находится в пределах нормы. Клинические и рентгенологические изменения в костях отсутствуют, либо наблюдается единичная плазмоцитома или остеопороз. Пациент может находиться на этой стадии в течение многих лет без необходимости в лечении.
- II стадия (умеренная масса). Уровень гемоглобина снижается до 85—100 г/л. Парапротеин lgG или lgA увеличивается до 5—7% и 3—5% соответственно. Концентрация бета-2-микроглобулина составляет 3,58−5,5 мг/л. Уровень кальция немного повышается. Начинают проявляться рентгенологические изменения в костях.
- III стадия (высокая масса). Уровень гемоглобина падает ниже 85 г/л. Парапротеин lgG и lgA повышается до 7% и 5% соответственно. Концентрация бета-2-микроглобулина составляет не менее 5,5 мг/л. Уровень кальция превышает 2,75 ммоль/л. Наблюдаются выраженные клинические проявления, включая остеолизис и три или более симптома поражения костей. Прогноз на этой стадии составляет не более 2—3 лет жизни.
Важно отметить, что хотя уровень бета-2-микроглобулина является значимым показателем для определения стадии миеломы, он может повышаться и по другим причинам, не связанным с этой болезнью, например, при диабете, гипертонии или нарушениях функции почек.
| Аспект заболевания | Описание | Значение для диагностики/лечения |
|---|---|---|
| Определение | Злокачественное заболевание плазматических клеток, характеризующееся их пролиферацией в костном мозге и выработкой моноклонального иммуноглобулина. | Понимание природы заболевания для выбора адекватной терапии. |
| Этиология | Точная причина неизвестна, но предполагаются генетические мутации, воздействие радиации, химических веществ, вирусов. | Выявление факторов риска для профилактики и ранней диагностики. |
| Патогенез | Накопление аномальных плазматических клеток в костном мозге, вытеснение нормальных кроветворных клеток, продукция парапротеина, вызывающего повреждение органов. | Объяснение клинических проявлений и разработка таргетной терапии. |
| Клинические проявления | Боль в костях, анемия, почечная недостаточность, гиперкальциемия, частые инфекции, неврологические нарушения. | Раннее распознавание симптомов для своевременного обращения к врачу. |
| Диагностика | Общий и биохимический анализ крови, анализ мочи, электрофорез белков сыворотки и мочи, биопсия костного мозга, рентгенография костей, МРТ, ПЭТ-КТ. | Подтверждение диагноза, определение стадии заболевания, оценка прогноза. |
| Стадирование | Используются системы стадирования (например, ISS, R-ISS) на основе уровня альбумина, бета-2-микроглобулина, ЛДГ, цитогенетических аномалий. | Определение тактики лечения и прогноза выживаемости. |
| Лечение | Химиотерапия, таргетная терапия, иммунотерапия, трансплантация стволовых клеток, лучевая терапия, поддерживающая терапия. | Выбор оптимального протокола лечения в зависимости от стадии и индивидуальных особенностей пациента. |
| Прогноз | Зависит от стадии заболевания, возраста пациента, наличия цитогенетических аномалий, ответа на лечение. | Информирование пациента о перспективах и планирование дальнейшего наблюдения. |
| Осложнения | Почечная недостаточность, патологические переломы, инфекции, гиперкальциемический криз, амилоидоз. | Профилактика и своевременное лечение осложнений для улучшения качества жизни. |
| Мониторинг | Регулярные анализы крови, мочи, инструментальные исследования для оценки эффективности лечения и выявления рецидивов. | Контроль за течением заболевания и своевременная коррекция терапии. |
Основные признаки
В результате увеличения количества плазматических клеток и производства моноклональных антител возникают симптомы миеломной болезни. Клинические проявления болезни можно описать следующим образом:
- Поражение костной ткани. Наиболее сильно страдают плоские кости и позвоночник. У пациентов возникают боли, а также возможны переломы. Костная ткань начинает разрушаться, и в самых тяжелых случаях может возникнуть угроза — сжатие спинного мозга, что можно выявить с помощью миелографии или МРТ.
- Амилоидоз почек. При миеломе в почечных канальцах увеличивается уровень белковых субъединиц иммуноглобулинов, которые откладываются в клубочках — скоплениях капилляров, через которые проходит кровь, образуя зернистые отложения.
- Анемия. У более чем половины пациентов с миеломой наблюдается снижение уровня гемоглобина и других форменных элементов крови.
- Повышенная восприимчивость к инфекциям. Большинство больных становятся более уязвимыми к бактериальным инфекциям из-за нарушенного образования и уменьшенного количества нормальных антител, а также дефектных нейтрофилов, что затрудняет их хемотаксис и миграцию. Хотя клеточный иммунитет обычно остается на нормальном уровне, летальные исходы при миеломной болезни часто происходят из-за инфекционных осложнений.
- Проблемы со свёртываемостью крови. Миелома может проявляться увеличением времени кровотечения, хотя такие случаи у пациентов встречаются довольно редко.
- Болезнь Рейно. Наличие аномальных белков криоглобулинов может привести к поражению мелких артерий и артериол, что вызывает цианоз верхних фаланг пальцев.
Лабораторная и инструментальная диагностика
Клинические проявления миеломной болезни достаточно ярко выражены, однако окончательное подтверждение наличия злокачественной опухоли из лимфоцитов возможно только на основе лабораторных исследований. Для диагностики применяются следующие методы:
- Общий анализ крови. Пониженный уровень гемоглобина и лейкоцитов, наряду с увеличением числа тромбоцитов и повышением скорости оседания эритроцитов, может указывать на наличие заболевания.
- Биохимический анализ крови. При миеломе наблюдается рост общего белка, вызванный специфическими иммуноглобулинами, а также повышение уровня кальция, креатинина, мочевины, лактадегидрогеназы и бета-2-микроглобулина.
- Иммунохимическое исследование крови и мочи. В случае заболевания выявляются аномальные белки класса lgG, реже lgA, lgD или lgE.
- Общий анализ мочи. Появление сывороточного парапротеина — белка Бенс-Джонса, который вырабатывается плазматическими клетками, служит признаком миеломной болезни.
- Пункция костного мозга. Если в образце костного мозга содержится более 10% плазматических клеток или они присутствуют в других тканях, это подтверждает диагноз миеломы. Эти клетки имеют округлую или овальную форму с эксцентрично расположенным ядром, хроматин внутри которого образует колесовидный узор, а цитоплазма может быть широкой и интенсивной синей окраски с четкими границами, с вакуолями или без них.
- Рентгенологическое исследование костей. Для миеломы характерно появление участков разрушенной костной ткани, а также очаги поражения черепа в виде гладкостенных пробоин и компрессионные переломы позвоночника.
- МРТ или КТ. Эти методы используются для дифференциальной диагностики с целью исключения других заболеваний костей и определения распространенности болезни.
Если миелома протекает бессимптомно (тлеющая форма), то поражения органов не наблюдаются. Тем не менее, диагноз ставится при уровне сывороточного парапротеина, превышающем 30 г/л, и по результатам пункции костного мозга, где выявляется более 10% плазматических клеток.
Если же показатели парапротеина и плазматических клеток составляют менее 30 г/л и 10% соответственно, заболевание классифицируется как моноклональная гаммапатия неопределенного значения.
https://youtube.com/watch?v=YQtJzJm76A0
Дополнительные исследования
Сходные признаки миеломы могут наблюдаться и у других злокачественных образований, таких как остеомиелит и лимфоплазмоцитарная лимфома. Для их исключения необходимы дополнительные исследования.
Костные метастазы могут развиваться при наличии злокачественной гемангиомы, заболеваниях лимфоидной ткани, а также при раке молочной железы или симпатической нервной системы. Основное отличие этих заболеваний от миеломы заключается в наличии первичного опухолевого очага, что подтверждается гистологическим анализом.
При остеомиелите наблюдается поражение трубчатых костей, а в крови возникает воспалительная реакция, что приводит к обнаружению гноя при биопсии. Кроме того, это заболевание чаще встречается у молодых людей, в отличие от миеломы.
Лимфоплазмоцитарная лимфома, которая вызывает увеличение лимфатических узлов и селезёнки, а также поражает костный мозг и лёгкие, характеризуется продукцией моноклонального протеина и крупных полипептидных субъединиц антител.
https://youtube.com/watch?v=JwJihc4sffY
Лечение химиотерапией
При значительном повышении уровня кальция, когда амилоидоз приводит к почечной недостаточности, наблюдается угнетение костно-мозгового кроветворения, возникают боли в костях, множественные поражения и патологические переломы, а также существует риск давления на спинной мозг, требуется применение химиотерапии. Она может проводиться по нескольким схемам:
- В самом простом варианте назначается монохимиотерапия с чередованием курсов цитостатиков. В этом случае используются препараты Мелфалан и Циклофосфамид. Мелфалан принимается в низких дозах (0,5 мг/кг) перорально в течение 4 дней с интервалом 4—6 недель и чередуется с регулярными внутривенными вливаниями по 16—20 мг/м2 каждые 2 недели. Циклофосфамид вводится внутримышечно в дозе 150—200 мг в сутки.
- Для пациентов с неблагоприятным прогнозом применяется полихимиотерапия. В этом случае используются не только Мелфалан и Циклофосфамид, но также Преднизолон, Винкристин, Доксорубицин или Дексаметазон. Тем не менее, существует мнение, что, несмотря на повышенную интенсивность, такая схема не увеличивает ни количество и продолжительность ремиссий, ни выживаемость.
- В период ремиссии после химиотерапии могут быть назначены препараты альфа-интерферона. При внутримышечном введении в дозе 3—6 миллионов единиц трижды в неделю, период улучшения может быть продлён. Интерферон эффективен как в комбинации с другими препаратами, так и в качестве монотерапии.
- У пациентов младше 65 лет чаще всего применяется высокодозная химиотерапия Мелфаланом с последующей трансплантацией донорского или собственного костного мозга. Этот подход позволяет значительно повысить безрецидивную и общую выживаемость.
Потенциальное излечение возможно только при успешной донорской трансплантации костного мозга. Однако данный метод ограничен возрастом пациента и высоким риском смертности (5—10%) из-за токсического воздействия самого лечения. Поэтому в большинстве случаев остаётся лишь контроль за течением заболевания и обеспечение длительной ремиссии.
https://youtube.com/watch?v=LH3SB2FeBp8
Другие методы
Если имеется единственный очаг разрастания плазматических клеток, возможно проведение хирургического вмешательства. Это также может быть рекомендовано в качестве дополнения к химиотерапии, если наблюдаются признаки сжатия жизненно важных органов, особенно спинного мозга. Хирургия в таких случаях включает удаление патологических образований или даже части позвоночника. В дополнение к этому назначаются глюкокортикоиды и лучевая терапия.
Лучевая терапия способствует улучшению качества жизни пациентов с ослабленным состоянием и обычно применяется в сочетании с другими методами лечения. Она становится необходимой при почечной недостаточности и устойчивости к химиотерапии. В качестве основного метода лечения лучевая терапия используется при локализованных поражениях костей.
Кроме того, необходимо проводить симптоматическое лечение, которое включает введение жидкостей и коррекцию гиперкальциемии, а также применение анальгетиков, гемостатической терапии и ортопедической помощи. Для остановки разрушения костной ткани и предотвращения переломов обычно используются препараты, такие как Памидронат, Золедроновая кислота или другие бисфосфонаты. В некоторых случаях при анемии может потребоваться назначение эритропоэтина и переливание эритроцитарной массы.
Созвучные заболевания
Миелома не должна быть спутана с острым миелоидным лейкозом (ОМЛ) или заболеваниями, связанными с повреждением миелиновой оболочки нервных волокон. При ОМЛ наблюдается подавление роста здоровых клеток крови из-за размножения аномальных лейкоцитов. Хотя лечение этого заболевания также в основном осуществляется с помощью химиотерапии, симптомы и методы диагностики ОМЛ и миеломной болезни значительно различаются.
Демиелинизирующие заболевания приводят к снижению проводимости нервных импульсов в поражённых нервах. Это может вызвать такие состояния, как рассеянный склероз, синдром Гийена-Барре и другие расстройства. Для диагностики разрушения миелиновой оболочки нейронов применяются методы МРТ и электромиография. Подход к лечению зависит от того, какие именно нарушения возникли в результате демиелинизации.
https://youtube.com/watch?v=qKPfD4KKMaU
Прогноз и выживаемость
Прогноз и выживаемость при миеломной болезни крови зависят от множества факторов, включая стадию заболевания, возраст пациента, общее состояние здоровья, а также ответ на проводимое лечение. Миеломная болезнь, также известная как множественная миелома, является злокачественным заболеванием, которое затрагивает плазматические клетки — тип белых кровяных клеток, ответственных за выработку антител. Изучение прогноза и выживаемости является важным аспектом в управлении этим заболеванием.
Согласно статистическим данным, средняя выживаемость пациентов с миеломной болезнью значительно улучшилась за последние десятилетия благодаря новым методам лечения, таким как иммунотерапия и таргетная терапия. В настоящее время средняя выживаемость составляет около 5-7 лет, однако у некоторых пациентов она может достигать 10 лет и более. Важно отметить, что эти цифры являются усредненными и могут варьироваться в зависимости от индивидуальных характеристик пациента.
Стадия заболевания на момент диагностики играет ключевую роль в прогнозе. Существует несколько систем классификации, наиболее распространенной из которых является система Durie-Salmon. Она делит миелому на стадии I, II и III, где III стадия характеризуется наиболее тяжелыми симптомами и худшим прогнозом. Пациенты с ранними стадиями заболевания, как правило, имеют более благоприятный прогноз и могут дольше оставаться в ремиссии.
Возраст пациента также является важным фактором. Исследования показывают, что молодые пациенты (до 65 лет) имеют более высокие шансы на успешное лечение и долгосрочную выживаемость по сравнению с пожилыми людьми. Это связано с тем, что у молодых пациентов, как правило, лучшее общее состояние здоровья и меньше сопутствующих заболеваний, что позволяет переносить более агрессивные методы лечения.
Ответ на лечение также является критически важным для оценки прогноза. Пациенты, у которых наблюдается полная или частичная ремиссия после первого курса терапии, имеют значительно лучшие шансы на долгосрочную выживаемость. В то же время, у пациентов с рецидивирующей миеломой или теми, кто не отвечает на лечение, прогноз может быть менее благоприятным.
Кроме того, генетические и молекулярные характеристики опухоли могут влиять на прогноз. Например, наличие определенных хромосомных аномалий, таких как делеции 17p или транслокации 4;14, может указывать на более агрессивное течение заболевания и худший прогноз. Современные методы молекулярной диагностики позволяют более точно оценить риск и адаптировать лечение в зависимости от индивидуальных особенностей заболевания.
В заключение, прогноз и выживаемость при миеломной болезни крови зависят от множества факторов, включая стадию заболевания, возраст пациента, ответ на лечение и молекулярные характеристики опухоли. С учетом прогресса в области диагностики и терапии, многие пациенты могут рассчитывать на улучшение качества жизни и увеличение продолжительности жизни, несмотря на наличие этого серьезного заболевания.
Психологические аспекты и поддержка пациентов
Миеломная болезнь крови, как и любое серьезное заболевание, оказывает значительное влияние не только на физическое состояние пациента, но и на его психологическое здоровье. Психологические аспекты, связанные с диагностикой и лечением миеломы, могут варьироваться от страха и тревоги до депрессии и социальной изоляции. Понимание этих аспектов является важной частью комплексного подхода к лечению и поддержке пациентов.
Первоначальная реакция на диагноз миеломной болезни часто включает в себя шок и отрицание. Пациенты могут испытывать трудности с принятием своего состояния, что может привести к эмоциональному стрессу. Важно, чтобы медицинские работники и близкие люди поддерживали пациента в этот трудный период, предоставляя информацию о заболевании и его лечении, а также предлагая эмоциональную поддержку.
Тревога и страх перед будущим — еще одни распространенные чувства, с которыми сталкиваются пациенты. Они могут беспокоиться о своем здоровье, финансовом состоянии, возможности продолжать работу и заботиться о семье. Эти переживания могут усугубляться неопределенностью, связанной с лечением и прогнозом заболевания. Психологическая поддержка, включая консультации с психотерапевтом или участие в группах поддержки, может помочь пациентам справиться с этими эмоциями и научиться управлять своим состоянием.
Депрессия является еще одним серьезным аспектом, который может возникнуть у пациентов с миеломной болезнью. Исследования показывают, что уровень депрессии у таких пациентов значительно выше, чем в общей популяции. Симптомы депрессии могут включать постоянное чувство грусти, потерю интереса к жизни, изменения в аппетите и сне. Важно, чтобы медицинские работники были внимательны к этим симптомам и предлагали соответствующую помощь, включая медикаментозное лечение и психотерапию.
Социальная изоляция также может стать проблемой для пациентов с миеломной болезнью. Из-за физического состояния и эмоционального стресса многие пациенты могут отдаляться от друзей и семьи, что усугубляет их состояние. Участие в группах поддержки, где пациенты могут общаться с теми, кто сталкивается с аналогичными проблемами, может помочь восстановить социальные связи и снизить чувство одиночества.
Семейная поддержка играет ключевую роль в процессе лечения. Близкие люди могут помочь пациенту справиться с эмоциональными трудностями, предоставляя поддержку и понимание. Важно, чтобы семья также заботилась о своем собственном эмоциональном состоянии, так как стресс, связанный с уходом за больным, может негативно сказаться на их здоровье.
В заключение, психологические аспекты миеломной болезни крови требуют внимательного подхода и поддержки как со стороны медицинских работников, так и со стороны близких. Комплексная поддержка, включающая психологическую помощь, участие в группах поддержки и активное вовлечение семьи, может значительно улучшить качество жизни пациентов и помочь им справиться с вызовами, связанными с заболеванием.
Исследования и новые подходы в терапии
Миеломная болезнь крови, также известная как множественная миелома, представляет собой злокачественное заболевание, которое возникает из плазматических клеток, находящихся в костном мозге. В последние годы в области диагностики и лечения миеломной болезни наблюдается значительный прогресс, что открывает новые горизонты для пациентов и врачей.
Одним из ключевых направлений исследований является изучение молекулярных механизмов, лежащих в основе миеломы. Ученые активно работают над идентификацией генетических мутаций и изменений в клеточном метаболизме, которые способствуют развитию заболевания. Это позволяет не только лучше понять патогенез миеломы, но и разрабатывать более целенаправленные и эффективные методы лечения.
В последние годы на передний план вышли новые классы препаратов, такие как ингибиторы протеасом, иммуно-модулирующие агенты и моноклональные антитела. Эти препараты продемонстрировали свою эффективность в клинических испытаниях и уже стали стандартом лечения для многих пациентов с миеломной болезнью. Например, такие препараты, как бортезомиб и леналидамид, значительно увеличивают продолжительность жизни и улучшают качество жизни пациентов.
Кроме того, активно исследуются подходы, основанные на использовании CAR-T клеток, которые представляют собой модифицированные Т-клетки, способные распознавать и уничтожать миеломные клетки. Первые результаты клинических испытаний показывают обнадеживающие данные о высокой эффективности и длительной ремиссии у пациентов, которые не поддаются традиционным методам лечения.
Не менее важным аспектом является персонализированный подход к терапии. Учитывая индивидуальные генетические особенности каждого пациента, врачи могут подбирать наиболее подходящие схемы лечения, что значительно повышает шансы на успешный исход. В этом контексте генетическое тестирование становится важным инструментом для определения прогноза и выбора терапии.
Также стоит отметить, что исследования в области миеломной болезни не ограничиваются только разработкой новых препаратов. Ученые активно изучают влияние сопутствующих заболеваний, таких как диабет и сердечно-сосудистые патологии, на течение миеломы и эффективность лечения. Это позволяет создать более комплексный подход к ведению пациентов, учитывающий все аспекты их здоровья.
В заключение, исследования и новые подходы в терапии миеломной болезни крови открывают новые возможности для пациентов. Применение современных методов диагностики и лечения, а также персонализированный подход к терапии позволяют значительно улучшить результаты лечения и качество жизни людей, страдающих от этого серьезного заболевания.